题目内容
下列操作中,能使电离平衡H2O H++OH-,向右移动且溶液呈酸性的是( )
H++OH-,向右移动且溶液呈酸性的是( )
A.向水中加入NaHSO4溶液 B.向水中加入Al2(SO4)3固体
C.向水中加入Na2CO3溶液 D.将水加热到100℃,使pH=6
【答案】
B
【解析】
试题分析:向水中加入NaHSO4溶液
,因为NaHSO4电离出大量的H+,抑制了水的电离,使得电离平衡H2O H++OH-,向左移动,虽然溶液呈酸性,但是不符合题意,故A不能选;向水中加入Al2(SO4)3固体
,铝离子水解,消耗了OH-,使得电离平衡H2O
H++OH-,向左移动,虽然溶液呈酸性,但是不符合题意,故A不能选;向水中加入Al2(SO4)3固体
,铝离子水解,消耗了OH-,使得电离平衡H2O H++OH-,向右移动且溶液呈酸性,所以B为本题的正确选项;向水中加入Na2CO3溶液,溶液呈现碱性,故C不能选;将水加热到100℃,能使电离平衡H2O
H++OH-,向右移动且溶液呈酸性,所以B为本题的正确选项;向水中加入Na2CO3溶液,溶液呈现碱性,故C不能选;将水加热到100℃,能使电离平衡H2O H++OH-,向右移动,pH=6,但是该溶液仍然呈现中性,故D不能选。
H++OH-,向右移动,pH=6,但是该溶液仍然呈现中性,故D不能选。
考点:电离平衡
点评:本题考查了电离平衡的基础知识,该考点是高考考查的重点和热点,本题难度适中。

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
 H++OH-,向右移动且溶液呈碱性的是( )
H++OH-,向右移动且溶液呈碱性的是( )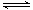 H++OH-,向右移动且溶液呈酸性的是( )
H++OH-,向右移动且溶液呈酸性的是( )