��Ŀ����
����Ŀ�������£���20 mLijŨ�ȵ���������μ���0.1 mol/L�İ�ˮ����ҺpH�ı仯����백ˮ�������ϵ��ͼ��ʾ��
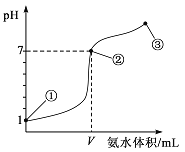
����������ȷ����
A. ��������ʵ���Ũ��Ϊl mol/L
B. ��������֮�������һ�㣺c(Cl-)��c(NH4+)��c(H+)��c(OH-)
C. �ڵ�����ʾ��Һ�У�c(NH4+)=c(Cl-)��c(OH-)=c(H+)����V<20
D. �ڵ�����ʾ��Һ�У���ˮ�������c(OH-)>l0-7mol/L
���𰸡�B
�����������������A����δ�Ӱ�ˮʱ�������pH=1��HCl��ǿ�������ȫ���룬�����ӵ�Ũ��=HCl��Ũ�ȣ�������������ʵ���Ũ��=0.1mol/L����A����B�����ü�ֵ����������δ�Ӱ�ˮʱ����Һ��û��笠����ӣ�����c(Cl-)��c(NH4+)������Һ�����ԣ��������ӵ�Ũ�ȴ������������ӵ�Ũ��c(H+)��c(OH-)����B��ȷ��C������Һ��PH=7ʱ����Һ��c(H+)=c(OH-)����Һ�ʵ����ԣ�����c(Cl-)=c(NH4+)���Ȼ����ǿ����������Һ�����ԣ�Ҫʹ��Һ�ʼ��ԣ���ˮ�����ʵ���Ӧ������һЩ����V��20����C����D����������Һ���Ǽ���Һ������ˮ�ĵ��룬������ʾ��Һ�ʼ��ԣ�������ˮ�ĵ��룬������ˮ�������c(OH-)��10-7mol/L����D����ѡB��

 ����ȫ���ִʾ��ƪ��ϵ�д�
����ȫ���ִʾ��ƪ��ϵ�д� �����߿����ϵ�д�
�����߿����ϵ�д�