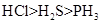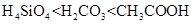题目内容
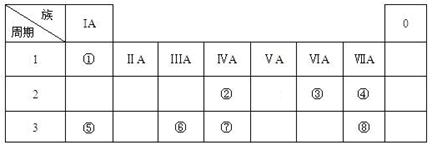
(13分)下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:① ,⑦ 。
(2)画出原子的结构示意图:④ ,⑧ ;
(3)在①~⑨元素中,原子半径最大的是(除稀有气体外) ,非金属性最强的元素是 ,最不活泼的元素是 。(均填元素名称)
(4)在①~⑨元素中的氢氧化物碱性最强的是 ;元素⑥、⑦、⑧的氢化物稳定性最弱的是 (均用化学式填空)
(5)第三周期中有一种元素,其最高价氧化物的水化物具有两性,用离子方程式表示该水化物分别与稀硫酸和烧碱溶液的反应:
与稀硫酸反应: ;
与烧碱溶液反应: 。
| | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | | | | | ① | | ② | |
| 三 | ③ | ④ | ⑤ | ⑥ | | ⑦ | ⑧ | ⑨ |
(2)画出原子的结构示意图:④ ,⑧ ;
(3)在①~⑨元素中,原子半径最大的是(除稀有气体外) ,非金属性最强的元素是 ,最不活泼的元素是 。(均填元素名称)
(4)在①~⑨元素中的氢氧化物碱性最强的是 ;元素⑥、⑦、⑧的氢化物稳定性最弱的是 (均用化学式填空)
(5)第三周期中有一种元素,其最高价氧化物的水化物具有两性,用离子方程式表示该水化物分别与稀硫酸和烧碱溶液的反应:
与稀硫酸反应: ;
与烧碱溶液反应: 。
(本小题共13分)
(1)(每空1分)① N ,⑦ S 。(2)(每空1分)④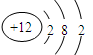 ,⑧
,⑧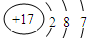
(3)(每空1分) 钠 , 氟 , 氩
(4)(每空1分) NaOH SiH4
(5)(每空2分)Al(OH)3+3H+ ="==" Al3+ + 3H2O Al(OH)3+OHˉ==AlO2–+ 2H2O
(1)(每空1分)① N ,⑦ S 。(2)(每空1分)④
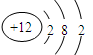 ,⑧
,⑧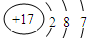
(3)(每空1分) 钠 , 氟 , 氩
(4)(每空1分) NaOH SiH4
(5)(每空2分)Al(OH)3+3H+ ="==" Al3+ + 3H2O Al(OH)3+OHˉ==AlO2–+ 2H2O
①~⑨对应的元素分别有: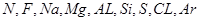 ,所以
,所以
(1)元素符号:①为N;⑦为S;
(2)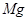 的原子结构示意图为:
的原子结构示意图为: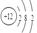 ;CL的原子结构示意图为:
;CL的原子结构示意图为: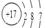 ;
;
(3)在①~⑨元素中,原子半径最大的是钠,非金属性最强的元素是氟,最不活泼的元素是氩;
(4)在①~⑨元素中的氢氧化物碱性最强的是NaOH;元素⑥、⑦、⑧的氢化物稳定性最弱的是SiH4;
(5)最高价氧化物的水化物具有两性的为氢氧化铝,对应的离子方程式为:
Al(OH)3+3H+ ="==" Al3+ + 3H2O;Al(OH)3+OHˉ==AlO2–+ 2H2O;
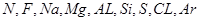 ,所以
,所以(1)元素符号:①为N;⑦为S;
(2)
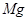 的原子结构示意图为:
的原子结构示意图为: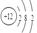 ;CL的原子结构示意图为:
;CL的原子结构示意图为: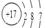 ;
;(3)在①~⑨元素中,原子半径最大的是钠,非金属性最强的元素是氟,最不活泼的元素是氩;
(4)在①~⑨元素中的氢氧化物碱性最强的是NaOH;元素⑥、⑦、⑧的氢化物稳定性最弱的是SiH4;
(5)最高价氧化物的水化物具有两性的为氢氧化铝,对应的离子方程式为:
Al(OH)3+3H+ ="==" Al3+ + 3H2O;Al(OH)3+OHˉ==AlO2–+ 2H2O;

练习册系列答案
相关题目