题目内容
铁元素及其化合物与人类的生产生活息息相关,
试回答下列问题:
(1)电子工业常用30%,的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板,写出该反应的离子方程式 。
(2)高炉炼铁过程中会发生反应:FeO(s)+CO(g) ![]() Fe(s)+CO2(g)。
Fe(s)+CO2(g)。
已知:Fe(s)+![]() O2(g)=FeO(s)△H=-272kJ·mol-1
O2(g)=FeO(s)△H=-272kJ·mol-1
C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1
2C(s)+O2(g)=2CO(g) △H=-22lkJ·mol-1
则:①FeO(s)+CO(g) ![]() Fe(s)+CO2(g) △H= 。
Fe(s)+CO2(g) △H= 。

②一定温度下,向某密闭容器中加人足量FeO,并充人一定量的CO气体,反应过程中CO和CO2的浓度与时间的关系如图所示
则从开始至达到平衡过程中,![]() (CO)= ;该温 度下,
(CO)= ;该温 度下,
FeO(s)+CO(g)![]() Fe(s)+CO2(g)
Fe(s)+CO2(g)
的化学平衡常数K= 。
(3)铁红是一种红色颜料,其成份是Fe2O3。将一定量的铁红溶于160mL5mol·L-1盐酸中,再加人一定量铁粉恰好完全溶解,收集到气体2.24L(标准状况),经检测,溶液中无Fe3+,则参加反应的铁粉的质量为 。
(1)2Fe3++Cu=2Fe2++Cu2+(2分)。
(2)①一1lkJ·mol-1(2分,漏掉或写错单位扣1分,漏掉“一”或数值错误不得分)②0625mol·L-1·min-1(2分,漏掉或写错单位扣1分);2(2分)
(3)11.2g(2分,漏掉或写错单位扣1分)

练习册系列答案
相关题目
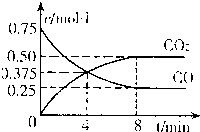 铁元素及其化合物与人类的生产生活息息相关,
铁元素及其化合物与人类的生产生活息息相关, O2(g)═FeO(s)△H=-272kJ?mol-1
O2(g)═FeO(s)△H=-272kJ?mol-1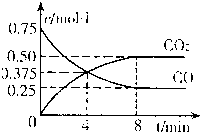
 O2(g)═FeO(s)△H=-272kJ?mol-1
O2(g)═FeO(s)△H=-272kJ?mol-1