题目内容
已知酸性高锰酸钾溶液可以将FeSO4氧化,方程式为2KMnO4+10FeSO4+ 8H2SO4=K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如下图所示。
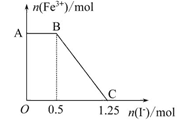
则下列有关说法不正确的是( )

则下列有关说法不正确的是( )
| A.图中AB段主要是高锰酸钾和碘化钾溶液反应 |
| B.图中BC段发生的反应为2Fe3++2I-=2Fe2++I2 |
| C.根据OC段的数据可知开始加入的高锰酸钾的物质的量为0.25 mol |
| D.向C点以后的溶液中加入少量KSCN溶液,溶液变红色 |
D
加入KI溶液后,AB段,Fe3+的物质的量不变,说明高锰酸钾溶液与硫酸亚铁溶液反应后高锰酸钾过量,根据电子守恒可知,过量的n(KMnO4)为0.5 mol÷5="0.1" mol。继续加入KI溶液,Fe3+的物质的量减少,发生反应2Fe3++2I-=2Fe2++I2,反应的n(Fe3+)="0.75" mol,所以生成0.75 mol Fe3+消耗的n(KMnO4)为0.75 mol÷5="0.15" mol,则开始加入的高锰酸钾的物质的量为0.25 mol。C点以后的溶液中不再含有Fe3+,加入少量KSCN溶液,溶液颜色不变

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
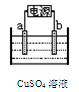

 =Fe3++2H2O+NO↑
=Fe3++2H2O+NO↑ 2Cu + O2↑+ 4H+
2Cu + O2↑+ 4H+ Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH- + CO32—→
+ CO32—→ + H2CO3
+ H2CO3 HCO3-+ H2O
HCO3-+ H2O