题目内容
11.在相同温度下,将H2和N2两种气体按不同比例通入相同的恒容密闭容器中,发生反应:3H2+N2?2NH3.$\frac{n{H}_{2}}{n{N}_{2}}$表示起始时H2和N2的物质的量之比,且起始时H2和N2的物质的量之和相等.下列图象正确的是( )| A. | 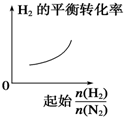 | B. | 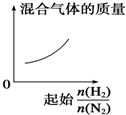 | C. | 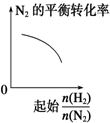 | D. | 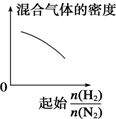 |
分析 A、随起始$\frac{n({H}_{2})}{n({N}_{2})}$增大,氢气量增大,依据平衡移动原理分析判断氢气的转化率;
B、随起始$\frac{n({H}_{2})}{n({N}_{2})}$增大,氢气量增大,混合气体质量减小;
C、随起始$\frac{n({H}_{2})}{n({N}_{2})}$增大,氢气量增大,氮气转化率增大;
D、随起始$\frac{n({H}_{2})}{n({N}_{2})}$增大,氢气量增大,混合气体质量减小,密度减小;
解答 解:A、随着起始$\frac{n({H}_{2})}{n({N}_{2})}$的增大,氢气含量增多,氢气的平衡转化率降低,故A错误;
B、随着起始$\frac{n({H}_{2})}{n({N}_{2})}$的增大,氢气含量增多,混合气体的质量减小,故B错误;
C、随着起始$\frac{n({H}_{2})}{n({N}_{2})}$的增大,氢气含量增多,氮气的平衡转化率增大,故C错误;
D、随着起始$\frac{n({H}_{2})}{n({N}_{2})}$的增大,氢气含量增多,混合气体的质量减小,则混合气体的密度减小,故D正确;
故选D.
点评 本题考查了化学平衡移动影响因素的分析判断,图象分析应用,掌握变化实质是解题关键,题目难度中等.

练习册系列答案
相关题目
1.下列说法中,错误的是( )
| A. | 能量变化是化学反应的基本特征之一 | |
| B. | 化学反应中能量变化的大小与反应物的质量多少无关 | |
| C. | 化学反应中必然伴随发生能量变化 | |
| D. | 化学变化中的能量变化主要是由化学键变化引起的 |
2.己烯是乙烯的同系物,常温下是无色的液体,难溶于水,比水轻.鉴别己烯、苯、四氯化碳三种无色液体,可选用的一种试剂是( )
| A. | 盐酸 | B. | 食盐水 | C. | 酒精 | D. | 溴水 |
19.空气是人类生存所必需的重要资源.为改善空气质量而启动的“蓝天工程”得到了全民的支持.下列措施不利于“蓝天工程”建设的是( )
| A. | 加大石油、煤炭的开采速度,增加化石燃料的供应量 | |
| B. | 推广使用燃煤脱硫技术,防治SO2污染 | |
| C. | 研制开发燃料电池汽车,消除机动车尾气污染 | |
| D. | 实施绿化工程,防治扬尘污染 |
6.下列说法正确的是( )
| A. | 在粗硅的制取中发生反应2C+SiO2$\frac{\underline{\;高温\;}}{\;}$2CO↑+Si,所以非金属性C>Si | |
| B. | 由Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$CO2↑+Na2SiO3可知硅酸的酸性大于碳酸 | |
| C. | 用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后再通入CO2 | |
| D. | 由H2S+CuSO4═CuS↓+H2SO4可知,氢硫酸的酸性比硫酸强 |
16.下列各组中两种微粒的半径(用r表示)之比小于1的是( )
| A. | $\frac{r(Na)}{r(N{a}^{+})}$ | B. | $\frac{r(S)}{r({S}^{2-})}$ | C. | $\frac{r(Mg)}{r(Al)}$ | D. | $\frac{r(Cl)}{r(F)}$ |
3.下列说法不正确的是( )
| A. | 正常雨水的pH为7.0,酸雨的pH小于7.0 | |
| B. | 严格执行机动车尾气排放标准有利于防止大气污染 | |
| C. | 使用二氧化硫和某些含硫化合物漂白食品会对人体健康产生危害 | |
| D. | PM 2.5是指大气中直径≤2.5微米的颗粒物,戴普通口罩还是对人体健康有影响 |
9.某恒容密闭容器中发生可逆反应:A(s)+B(g)?C(g),能说明该反应已达到平衡状态的是( )
| A. | 容器内A、B、C三者共存 | B. | vC=vB | ||
| C. | 容器内压强不再变化 | D. | 气体的密度不再变化 |
 .
.