��Ŀ����
��һ���ݻ�����ķ�Ӧ���У�Ҫ�������ϵ���¶�ʹ���з�Ӧ�ﵽƽ��ʱ����������������������ʵ���Ϊ12 mol��
��֪��ӦA(g)+2B(g) 2C(g)�����������м���6.5 mol A��x mol B��2.0 mol C��
2C(g)�������������6.5 mol A��x mol B��2.0 mol C��
��1����x=5.5ʱ����Ҫ������ϵ���¶�ʹ��Ӧ��ƽ��ʱ�ﵽ����������������ӦΪ_______������ȡ����ȡ�����Ӧ��
��2����ʹ��ʼ��Ӧά�����淴Ӧ������У���x��ȡֵ��ΧΪ_________��
��3����һ���¶��µ�����ƽ����ϵ�У�����1��2 �����ʵ���֮��ͨ��D��E�������壨��ʱ����������������ʵ�����Ҫ��12 mol��������ʽ��Ӧ��D(g)+E(g) 2F(g),����Ӧ�ﵽƽ��ʱ��D�������������е��������Ϊp%������������Ͷ��m mol D\,n mol F��һ������E���������������µ�ƽ����ϵ�У�D�����������Ϊp%����Ͷ��E�����ʵ���Ϊ________mol����A��B��C��D��E��F֮�������Ӧ����
2F(g),����Ӧ�ﵽƽ��ʱ��D�������������е��������Ϊp%������������Ͷ��m mol D\,n mol F��һ������E���������������µ�ƽ����ϵ�У�D�����������Ϊp%����Ͷ��E�����ʵ���Ϊ________mol����A��B��C��D��E��F֮�������Ӧ����
��֪��ӦA(g)+2B(g)
 2C(g)�������������6.5 mol A��x mol B��2.0 mol C��
2C(g)�����������м���6.5 mol A��x mol B��2.0 mol C����1����x=5.5ʱ����Ҫ������ϵ���¶�ʹ��Ӧ��ƽ��ʱ�ﵽ����������������ӦΪ_______������ȡ����ȡ�����Ӧ��
��2����ʹ��ʼ��Ӧά�����淴Ӧ������У���x��ȡֵ��ΧΪ_________��
��3����һ���¶��µ�����ƽ����ϵ�У�����1��2 �����ʵ���֮��ͨ��D��E�������壨��ʱ����������������ʵ�����Ҫ��12 mol��������ʽ��Ӧ��D(g)+E(g)
 2F(g),����Ӧ�ﵽƽ��ʱ��D�������������е��������Ϊp%������������Ͷ��m mol D\,n mol F��һ������E���������������µ�ƽ����ϵ�У�D�����������Ϊp%����Ͷ��E�����ʵ���Ϊ________mol����A��B��C��D��E��F֮�������Ӧ����
2F(g),����Ӧ�ﵽƽ��ʱ��D�������������е��������Ϊp%������������Ͷ��m mol D\,n mol F��һ������E���������������µ�ƽ����ϵ�У�D�����������Ϊp%����Ͷ��E�����ʵ���Ϊ________mol����A��B��C��D��E��F֮�������Ӧ������1�����ȣ�2��2.5��x��3.5
(3)2m+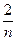
(3)2m+
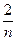
��1�� A(g) + 2B(g) 2C(g)
2C(g)
��ʼ/mol 6.5 x 2
ƽ��n��="12" mol
��x=5.5ʱ��6.5+5.5+2=13��12,����ʹƽ�������ƶ���ʹn��="12" mol,������ӦΪ���ȷ�Ӧ��
��2����ά�ַ�Ӧ���淴Ӧ������У����У�
6.5+x+2��12������x��3.5��
��Cת����a mol��
A(g) + 2B(g) 2C(g)
2C(g)
��ʼ6.5 x 2
ƽ��6.5+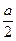 x+a 2-a
x+a 2-a
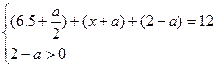
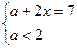 ����x��2.5
����x��2.5
��x��ȡֵ��Χ��2.5��x��3.5��
(3)���з�Ӧ��D(g) + E(g) 2F(g)
2F(g)
��ʼ�� m n(E) n
��ƽ�⣺��m+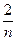 ���ã�n(E)+
���ã�n(E)+ 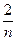 ��=1��2��
��=1��2��
�����ǵ������Ӧ�����֣�m+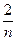 ���ã�n(E)+
���ã�n(E)+ 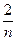 ��=1��2����,n(E)=2m+
��=1��2����,n(E)=2m+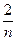 ��
��
 2C(g)
2C(g)��ʼ/mol 6.5 x 2
ƽ��n��="12" mol
��x=5.5ʱ��6.5+5.5+2=13��12,����ʹƽ�������ƶ���ʹn��="12" mol,������ӦΪ���ȷ�Ӧ��
��2����ά�ַ�Ӧ���淴Ӧ������У����У�
6.5+x+2��12������x��3.5��
��Cת����a mol��
A(g) + 2B(g)
 2C(g)
2C(g)��ʼ6.5 x 2
ƽ��6.5+
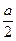 x+a 2-a
x+a 2-a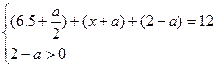
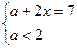 ����x��2.5
����x��2.5��x��ȡֵ��Χ��2.5��x��3.5��
(3)���з�Ӧ��D(g) + E(g)
 2F(g)
2F(g)��ʼ�� m n(E) n
��ƽ�⣺��m+
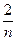 ���ã�n(E)+
���ã�n(E)+ 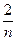 ��=1��2��
��=1��2�������ǵ������Ӧ�����֣�m+
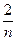 ���ã�n(E)+
���ã�n(E)+ 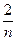 ��=1��2����,n(E)=2m+
��=1��2����,n(E)=2m+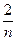 ��
��
��ϰ��ϵ�д�
�����Ŀ
 pC(g)��ƽ�����һ���¶��£������������С��ԭ����1/2�����ﵽ��ƽ���C��Ũ��Ϊԭ����1.9������ѹ���������¶ȱ��ֲ��䣬������˵����ȷ���ǣ�����
pC(g)��ƽ�����һ���¶��£������������С��ԭ����1/2�����ﵽ��ƽ���C��Ũ��Ϊԭ����1.9������ѹ���������¶ȱ��ֲ��䣬������˵����ȷ���ǣ�����
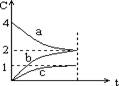
 pC��g)�ﵽƽ���ѹ�����������������A��ת������֮���͡�����˵����ȷ���ǣ� ��
pC��g)�ﵽƽ���ѹ�����������������A��ת������֮���͡�����˵����ȷ���ǣ� ��
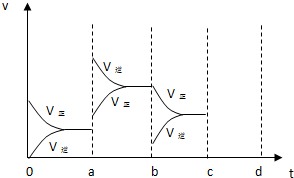
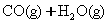

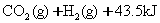 �ķ�Ӧ�иı������ĸ�����������ʹ����Ӧ����������ǣ� ����
�ķ�Ӧ�иı������ĸ�����������ʹ����Ӧ����������ǣ� ���� H2(g)+I2��g���Ѵ�ƽ�⣬���������С������С�Ĺ����У�
H2(g)+I2��g���Ѵ�ƽ�⣬���������С������С�Ĺ����У�