题目内容
【题目】下列离子方程式,一定不正确的是.( )
A.实验室用石灰石和盐酸反应制取CO2:CaCO3+2H+═Ca2++CO2↑+H2O
B.H2O2溶液中滴加酸性KMnO4溶液:2MnO ![]() +5H2O2+6H+═2Mn2++5O2↑+8H2O
+5H2O2+6H+═2Mn2++5O2↑+8H2O
C.铁屑溶于过量稀硝酸:3Fe+8H++2NO ![]() ═3Fe2++2NO↑+4H2O
═3Fe2++2NO↑+4H2O
D.NaHCO3溶液与足量Ba(OH)2溶液反应:HCO ![]() +Ba2++OH﹣═BaCO3↓+H2O
+Ba2++OH﹣═BaCO3↓+H2O
【答案】C
【解析】解:A.实验室用石灰石和盐酸反应制取CO2的离子反应为CaCO3+2H+═Ca2++CO2↑+H2O,故A正确;B.H2O2溶液中滴加酸性KMnO4溶液的离子反应为2MnO ![]() +5H2O2+6H+═2Mn2++5O2↑+8H2O,故B正确;
+5H2O2+6H+═2Mn2++5O2↑+8H2O,故B正确;
C.铁屑溶于过量稀硝酸的离子反应为Fe+4H++NO ![]() ═Fe3++NO↑+2H2O,故C错误;
═Fe3++NO↑+2H2O,故C错误;
D.NaHCO3溶液与足量Ba(OH)2溶液反应的离子反应为HCO ![]() +Ba2++OH﹣═BaCO3↓+H2O,故D正确;
+Ba2++OH﹣═BaCO3↓+H2O,故D正确;
故选C.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯 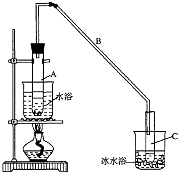
已知: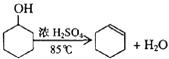
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | ﹣103 | 83 | 难溶于水 |
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入l mL浓硫酸,摇匀后放入碎瓷片,
缓慢加热至反应完全,在试管C内得到环己烯粗品.
①A中碎瓷片的作用是 , 导管B除了导气外还具有的作用是 .
②试管C置于冰水浴中的目的是 .
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等.加入饱和食盐水,振荡、静 置、分层,环己烯在上层,分液后用(填入编号)洗涤.
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②实验制得的环己烯精品的质量往往低于理论产量,其可能的原因是
a.蒸馏时从100℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是 . a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点.