��Ŀ����
ij����ѧϰС����ճ������в���ȱ�ٵĵ�ζƷM����̽������֪C����D��ȼ�շ�����ɫ���森M���������ʵ�ת����ϵ��ͼ��ʾ�����ֲ�������ȥ����

��1��д��F�ĵ���ʽ ��
��2����A��һ�ֳ���������������ҿ��������첣����E��Һ��F��Һ��Ӧ�����Ʊ�һ�ֽ��壬��E��Һ���׳���___________
��3����A��CO2���壬A��B��Һ�ܹ���Ӧ����Ӧ�����õ���Һ�������ᷴӦ����ͼ��ʾ����A��B��Һ��Ӧ����Һ�е����ʻ�ѧʽΪ ��
��4����A��һ�ֳ����������ʣ���A��B��Һ�ܹ���Ӧ��������F��Һ��μ���E��Һ���ӱ�����������ʵ�������� ��
��5����A��һ�ֻ��ʣ�ʵ���ҿ���A��B��Ӧ��ȡ����E��E��F��E��D������ð���̣�������E ��D�ķ�Ӧ��������D�Ĺܵ��Ƿ�й¶��д��E��D��Ӧ�Ļ�ѧ����ʽ�� ��

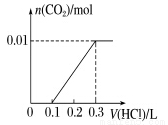
��6����A��һ����Һ��ֻ���ܺ���H+��NH4+��Mg2+��Fe3+��Al3+��CO32����SO42���е�ijЩ���ӣ��������Һ�м���B��Һʱ�������ɳ��������ʵ�����B��Һ����������仯��ͼ.��ʾ���ɴ˿�֪������Һ�п϶����е����Ӽ���Ũ��֮��Ϊ ��
H2O2�㷺Ӧ���ڻ�ѧƷ�ϳɡ�ֽ���ͷ�֯Ʒ��Ư�ף��ǻ�����Һ��Ư�������о�������H2O2��Һ��Ư������HO2�����¡�
��1�� H2O2��Һ��������,���0.15 mol��L?1 H2O2��ҺpHԼΪ6��д��H2O2����HO2���ĵ��뷽��ʽ�� ��
��2������������ͬʱ���о���ͬ��ʼpH������H2O2��Һ��Ư��Ч����������£�

����ͼ�ɵõ��Ľ����� �����ƽ���ƶ�ԭ���������ɣ� ��
��3��ʵ�鷢�֣� ��pH >11����H2O2��Һ��Ư��Ч����pH��������͡������һ����������ʵ�飬������Һ��H2O2�ķֽ���pH�йء��ⶨ��ͬ��ʼpH�����£���ʼŨ�Ⱦ�Ϊ0.15 mol��L?1 ��H2O2��Һ�����ֽⷴӦ��������£�
��ʼpH | pH = 10 | pH = 12 |
1Сʱ��H2O2��ҺŨ�� | 0.13 mol��L?1 | 0.07 mol��L?1 |
1Сʱ��pH | û�����Ա仯 | û�����Ա仯 |
�������ϣ�HO2��+H2O2=H2O+O2+OH����
�ٽ�����ӷ���ʽ����1Сʱ��pHû�����Ա仯��ԭ�� ��
�ڴӷ�Ӧ���ʵĽǶȷ���pH����H2O2��ҺƯ��Ч���ή�͵�ԭ�� ��


 N2(g)+2CO2(g) ��H = ��746 kJ��mol��1
N2(g)+2CO2(g) ��H = ��746 kJ��mol��1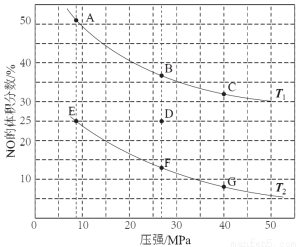
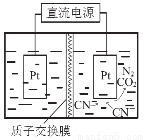
 4Ag+O2��+4H+
4Ag+O2��+4H+