题目内容
3.下列各组物质中,化学键的类型完全相同的是( )| A. | H2S、MgCl2 | B. | NH3、CO2 | C. | CaCl2、NaOH | D. | H2O2、Na2O2 |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,铵盐中存在离子键,以此解答该题.
解答 解:A.H2S存在共价键,MgCl2存在离子键,故A错误;
B.NH3、CO2都为共价化合物,存在共价键,故B正确;
C.CaCl2含有离子键,NaOH含有离子键和共价键,故C错误;
D.H2O2含有离子键,Na2O2含有离子键和共价键,故D错误.
故选B.
点评 本题考查了离子键和共价键的判断,为高频考点,侧重考查学生的分析能力,根据物质构成微粒及微粒间作用力分析解答即可,答题时注意不能根据是否含有金属元素判断离子键,并不是所有物质都含有化学键,稀有气体不含化学键,为易错点,题目难度不大.

练习册系列答案
相关题目
1.下列说法中正确的是( )
| A. | 将纯水加热的过程中,KW变大,酸性增强 | |
| B. | 保存FeSO4溶液时,加入稀HNO3抑制Fe2+水解 | |
| C. | NaHCO3溶液蒸干、灼烧至恒重,最终得到NaHCO3固体 | |
| D. | 相同浓度的下列溶液中:①CH3COONH4、②CH3COONa、③CH3COOH中,c(CH3COCO-)由大到小的顺序是②>①>③ |
2.钡与钠相似,也能形成含O22-的过氧化物,下列叙述正确的是( )
| A. | 金属钡和硫酸铜溶液的反应:Ba+CuSO4═BaSO4↓+Cu | |
| B. | 过氧化钡的化学式为Ba2O2 | |
| C. | 反应Na2O2+2HCl═2NaCl+H2O2为氧化还原反应 | |
| D. | 过氧化钡和过氧化钠都具有强氧化性 |
8. 如图是一套实验制取气体的装置,用于发生、干燥和收集气体.下列各组物质中能利用这套装置进行实验的是
如图是一套实验制取气体的装置,用于发生、干燥和收集气体.下列各组物质中能利用这套装置进行实验的是
( )
 如图是一套实验制取气体的装置,用于发生、干燥和收集气体.下列各组物质中能利用这套装置进行实验的是
如图是一套实验制取气体的装置,用于发生、干燥和收集气体.下列各组物质中能利用这套装置进行实验的是 ( )
| A. | 铜屑和稀硝酸 | B. | 碳酸钙和稀盐酸 | ||
| C. | 二氧化锰和浓盐酸 | D. | 氧化钙和浓氨水 |
15.已知:将乙醇和浓硫酸反应的温度控制在140℃,乙醇会发生分子间脱水,并生成乙醚,其反应方程式为:
2C2H5OH$→_{140℃}^{浓H_{2}SO_{4}}$C2H5-O-2C2H5+H2O,用浓硫酸与分子式分别为C2H6O和C3H8O的醇的混合液反应,可以得到醚的种类有( )
2C2H5OH$→_{140℃}^{浓H_{2}SO_{4}}$C2H5-O-2C2H5+H2O,用浓硫酸与分子式分别为C2H6O和C3H8O的醇的混合液反应,可以得到醚的种类有( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
12.下列化学用语正确的是( )
| A. | 乙醇分子的结构式: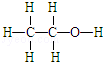 | B. | 氯原子的结构示意 | ||
| C. | 过氧化氢分子的电子式: | D. | 乙烯的最简式:C2H4 |

 $→_{②H+/H_{2}O}^{①HCN}$
$→_{②H+/H_{2}O}^{①HCN}$

 $\stackrel{-H_{2}O}{→}$(CH3)3CCHO=CHCHO
$\stackrel{-H_{2}O}{→}$(CH3)3CCHO=CHCHO .
. .
. .
.