题目内容
下列说法正确的是( )
| A.甲烷的标准燃烧热为ΔH=-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为 CH4(g)+2O2(g)=CO2(g)+2H2O(g)ΔH=-890.3 kJ·mol-1 |
| B.已知H2O(L)=H2O(g) ΔH=+44kJ·mol-1,则2g H2(g)完全燃烧生成液态水比生成 气态水多释放22kJ的能量 |
| C.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的ΔH<0 |
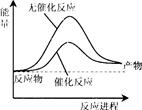
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的ΔH相同 |
D
试题分析:燃烧热是在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,A不正确,因为水的稳定状态是液态;B中2g氢气是1mol,可以生成1mol水,即18g水,所以2g H2(g)完全燃烧生成液态水比生成气态水多释放44kJ的能量,B不正确;C不正确,该反应水吸热反应。反应热和反应条件无关系,D正确,答案选D。
点评:该题是高考中的常见题型,属于中等难度的试题。试题针对性强,贴近高考,旨在培养学生灵活运用基础知识解决实际问题的能力。该题的关键是明确反应热、燃烧热以及反应自发性的含义以及判断依据,然后灵活运用即可。

练习册系列答案
相关题目
 2NH3(g)△H=" —92" kJ/mol,相关数据如下表。一定条件下,在体积为1L的密闭容器中加入1molN2和3molH2充分反应,放出热量Q1kJ,下列说法正确的是( )
2NH3(g)△H=" —92" kJ/mol,相关数据如下表。一定条件下,在体积为1L的密闭容器中加入1molN2和3molH2充分反应,放出热量Q1kJ,下列说法正确的是( )