题目内容
【题目】在 300 mL 2 mol/L H2SO4溶液中,SO![]() 的物质的量浓度是多少?H+的物质的量浓度是多少?溶质的质量是多少?此溶液中含 H+的物质的量是少?其中含有多少个 SO
的物质的量浓度是多少?H+的物质的量浓度是多少?溶质的质量是多少?此溶液中含 H+的物质的量是少?其中含有多少个 SO![]() ?
?
【答案】2mol/L;4mol/L;58.8g;1.2mol;3.612×1023
【解析】
300 mL 2 mol/L H2SO4溶液中,c(SO![]() )=c(H2SO4)= 2 mol/L;
)=c(H2SO4)= 2 mol/L;
c(H+)= 2 c(H2SO4)= 4 mol/L;
溶质即 H2SO4,由于n (H2SO4) = 0.3 L×2 mol/L = 0.6 mol,所以m(H2SO4) = 98 g/mol×0.6 mol = 58.8 g;
n(H+)= 2n(H2SO4)= 1.2 mol;
n(SO![]() )= 0.6 mol,根据
)= 0.6 mol,根据![]() 可知N(SO
可知N(SO![]() )= 0.6 mol×6.02×1023mol-1= 3.612×1023。
)= 0.6 mol×6.02×1023mol-1= 3.612×1023。

练习册系列答案
相关题目
【题目】在容积一定的密闭容器中发生可逆反应A(g)+B(g)![]() C(g)H>0,平衡移动关系如图所示。下列说法正确的是( )
C(g)H>0,平衡移动关系如图所示。下列说法正确的是( )
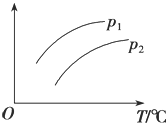
选项 | 压强 | 纵坐标 |
A | p1<p2 | C的物质的量浓度 |
B | p1>p2 | B的转化率 |
C | p1<p2 | 混合气体的平均摩尔质量 |
D | p1>p2 | A的质量分数 |
A.AB.BC.CD.D