题目内容
同温同压下,等质量的二氧化硫和二氧化碳相比较,下列叙述中正确的是( )A.氧原子数之比为16:11
B.密度比为11:16
C.体积比为1:1
D.体积比为11:16
【答案】分析:根据质量相同计算出两种物质的物质的量之比,结合阿伏加德罗定律及其推论计算并比较氧原子数、密度、体积的关系.
解答:解:设两种物质的质量都为1g,则SO2和CO2的物质的量之比为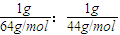 =11:16.
=11:16.
A、每个二氧化硫分子和二氧化碳分子中含有的氧原子数都是2个,所以二氧化硫和二氧化碳中含有的氧原子数之比等于其物质的量之比11:16,故A错误;
B、同温同压下,气体摩尔体积相同,相同质量的二氧化硫和二氧化碳其密度之比=ρ(SO2):ρ(CO2)=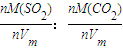 =64:44=16:11,故B错误;
=64:44=16:11,故B错误;
C、同温同压下,气体的体积之比等于物质的量之比,则SO2和SO2的体积之比为V(SO2):V(SO2)=11:16,故C错误;
D、同温同压下,气体的体积之比等于物质的量之比,则SO2和SO2的体积之比为V(SO2):V(SO2)=11:16,故D正确;
故选D.
点评:本题考查物质的量的相关计算以及阿伏加德罗定律及其推论的有关知识,题目难度不大,注意有关公式的利用.
解答:解:设两种物质的质量都为1g,则SO2和CO2的物质的量之比为
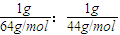 =11:16.
=11:16.A、每个二氧化硫分子和二氧化碳分子中含有的氧原子数都是2个,所以二氧化硫和二氧化碳中含有的氧原子数之比等于其物质的量之比11:16,故A错误;
B、同温同压下,气体摩尔体积相同,相同质量的二氧化硫和二氧化碳其密度之比=ρ(SO2):ρ(CO2)=
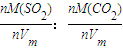 =64:44=16:11,故B错误;
=64:44=16:11,故B错误;C、同温同压下,气体的体积之比等于物质的量之比,则SO2和SO2的体积之比为V(SO2):V(SO2)=11:16,故C错误;
D、同温同压下,气体的体积之比等于物质的量之比,则SO2和SO2的体积之比为V(SO2):V(SO2)=11:16,故D正确;
故选D.
点评:本题考查物质的量的相关计算以及阿伏加德罗定律及其推论的有关知识,题目难度不大,注意有关公式的利用.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
同温同压下,等质量的O2和CO2相比较,下列叙述正确的是( )
| A.体积比为8:11 | B.分子个数之比为11: 12 |
| C.物质的量之比为8:11 | D.原子个数之比为11: 12 |
同温同压下,等质量的O2和CO2相比较,下列叙述正确的是:
| A.体积比为8:1 | B.分子个数之比为11:12 |
| C.物质的量之比为8:11 | D.原子个数之比为11:12 |