题目内容
8.判断下列有关化学基本概念的依据正确的是( )| A. | 溶液与胶体:不同的本质原因是能否发生丁达尔效应 | |
| B. | 电解质与非电解质:物质本身的导电性 | |
| C. | 氧化还原反应:反应前后元素化合价是否变化 | |
| D. | 纯净物与混合物:是否仅含有一种元素 |
分析 A.溶液和胶体的本质区别在于分散质粒子直径的大小;
B.导电的不一定是电解质;
C.氧化还原反应的本质是有电子的得失或偏移,表现为有化合价的升降;
D.仅含一种元素的不一定是纯净物.
解答 解:A.分散系根据分散质粒子直径的大小可以分为溶液、胶体和浊液.所以溶液和胶体的本质区别是分散质粒子直径的大小.故A错误;
B.电解质:在水溶液中或熔融状态下能导电的化合物;非电解质:在水溶液中和熔融状态下均不能导电的化合物.根据定义可以看出,电解质、非电解质的判断并不是看物质本身是否导电,而是看在在水溶液中或熔融状态下是否能导电,故B错误;
C.氧化还原反应的本质是有电子的得失或偏移,表现为有化合价的升降,故根据反应前后元素化合价是否变化可以判断是否是氧化还原反应,故C正确;
D.纯净物:只由一种物质组成的称为纯净物.混合物:由两种或两种以上物质组成的称为混合物.所以纯净物、混合物与是否仅含一种元素没有必然的关系.比如:O2和O3混合在一起,虽然只含一种元素,但仍是混合物;H2SO4含三种元素,但由于是一种物质,故仍是纯净物,故D错误.
故选C.
点评 本题考查了常见化学概念的判断依据,容易出错的是电解质、非电解质的判断依据,应注意掌握,题目难度不大.

练习册系列答案
相关题目
18.下列事实中,能证实一元酸HR是弱电解质的是( )
| A. | HR溶液和KCl溶液不发生反应 | |
| B. | 能与水以任意比例互溶 | |
| C. | 0.1 mol•L-1 的HR溶液中c(R- )=0.01 mol•L-1 | |
| D. | HR属于共价化合物 |
19.已知弱电解质在水中的电离平衡常数(25℃)如表:
现有常温下0.1mol•L-1的(NH4)2CO3溶液.
①你认为该溶液呈碱性(填“酸”“中”“碱”).
②就该溶液中粒子之间有下列关系式,你认为其中正确的是ACD
A.c(NH4+)>c(CO32-)>c(HCO3-)>c(NH3•H2O)
B.c(NH4+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-)
C.c(CO32-)+c(HCO3-)+c(H2CO3)=0.1mol•L-1
D.c(NH4+)+c(NH3•H2O)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
| 弱电解质 | H2CO3 | NH3•H2O |
| 电离平衡常数 | Ka1=4.30×10-7 Ka2=5.61×10-11 | 1.77×10-5 |
①你认为该溶液呈碱性(填“酸”“中”“碱”).
②就该溶液中粒子之间有下列关系式,你认为其中正确的是ACD
A.c(NH4+)>c(CO32-)>c(HCO3-)>c(NH3•H2O)
B.c(NH4+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-)
C.c(CO32-)+c(HCO3-)+c(H2CO3)=0.1mol•L-1
D.c(NH4+)+c(NH3•H2O)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
16.下列哪种物质常用于保护食物,以免被微生物侵蚀腐败( )
| A. | 酒精 | B. | 食盐 | C. | 醋酸 | D. | 硝酸钾 |
20.已知氯气和NaOH在一定温度下能发生反应:Cl2+2NaOH=NaCl+NaClO+H2O,3Cl2+6NaOH=5NaCl+NaClO3+3H2O.某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液.经测定ClO-与ClO3-的物质的量之比为1:3,则氯气与氢氧化钠反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为( )
| A. | 21:5 | B. | 11:3 | C. | 3:1 | D. | 4:1 |
18.下列说法正确的是( )
| A. | 硫酸亚铁与氢氧化钠溶液混合生成氢氧化亚铁和硫酸钠的反应属于氧化还原反应 | |
| B. | Fe0与一氧化碳反应得到单质铁属于置换反应 | |
| C. | 在自然界中不存在铁单质 | |
| D. | 炽热的铁丝在充满氧气的集气瓶中发生化合反应 |
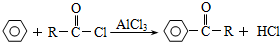
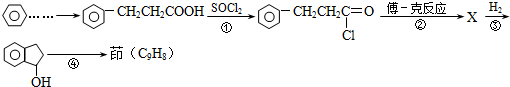
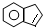 .
.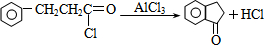 .
.