题目内容
能正确表示下列反应的离子方程式是
CO32-+2H2O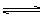 H2CO3+2OH-
H2CO3+2OH-
| A.铜跟浓硝酸反应: Cu+4HNO3=Cu2++2NO3-+2NO2↑+2H2O |
B.二氧化锰与浓盐酸反应(加热):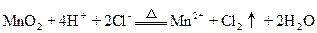 |
C.电解硫酸铜溶液(用惰性电极):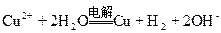 |
| D.纯碱与水反应: |
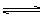 H2CO3+2OH-
H2CO3+2OH-B
A.错误。浓HNO3的质量分数69%左右,水量仍很大,所以HNO3以离子形式存在。所以正确表示为:
Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O
B.正确。浓盐酸的浓度为37%,所以HCl以离子形式存在。
C.错误。电极反应有误。在阳极上应是OH-失电子放电生成O2。即
阳极:4OH--4e=O2↑+2H2O;阴极:Cu2++2e=Cu
总反应:2Cu2++2H2O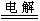 2Cu+O2↑+4H+
2Cu+O2↑+4H+
D.错误。CO32-水解是分步进行的,其中以第一步为主,第二步极微量,故两步不可合并。正确表示为:CO32-+H2O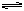 HCO3-+OH-
HCO3-+OH-
Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O
B.正确。浓盐酸的浓度为37%,所以HCl以离子形式存在。
C.错误。电极反应有误。在阳极上应是OH-失电子放电生成O2。即
阳极:4OH--4e=O2↑+2H2O;阴极:Cu2++2e=Cu
总反应:2Cu2++2H2O
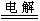 2Cu+O2↑+4H+
2Cu+O2↑+4H+D.错误。CO32-水解是分步进行的,其中以第一步为主,第二步极微量,故两步不可合并。正确表示为:CO32-+H2O
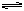 HCO3-+OH-
HCO3-+OH-
练习册系列答案
相关题目
 Ca2++
Ca2++
 S2-+H3O+
S2-+H3O+ 4FeCl3+2FeBr3,则16.8 L Cl2(标准状况)通入250 mL 3 mol·L-1的FeBr2溶液中,发生反应的离子方程式正确的是( )?
4FeCl3+2FeBr3,则16.8 L Cl2(标准状况)通入250 mL 3 mol·L-1的FeBr2溶液中,发生反应的离子方程式正确的是( )?

