题目内容
(12分)用Na2CO3固体配制1mol/L的Na2CO3溶液100mL。
(1)供选用的仪器有:①玻璃棒;②胶头滴管;③酒精灯;④100mL容量瓶;⑤250mL量筒;⑥天平;⑦50mL烧杯;应选用的仪器(填编号) 。
(2)应称取Na2CO3的质量为 g;若称量时砝码和物品放反了,则实际称量的Na2CO3的质量为 g 。
(3)下列操作,会引起所配溶液浓度偏高的是( )
| A.称取的Na2CO3固体中有杂质 |
| B.溶解Na2CO3固体时,因搅拌剧烈使烧杯中的溶液溅出少量 |
| C.没有洗涤烧杯及玻璃棒 |
| D.定容时发现液面高于刻度线,用胶头滴管吸出多余的溶剂 |
F、定容时俯视刻度线
G、定容摇匀后,发现液面低于刻度线,再加至刻度线
(4)取所配Na2CO3溶液20ml,向其中滴加足量的稀盐酸,可得到标况下的气体 L,将得到的气体全部通入足量的澄清石灰水,充分反应后,将沉淀过滤,洗涤,干燥,最后可得固体 g。
(1)①②④⑥⑦ (2)10.6;9.4 (3)F (4)0.448; 2
解析试题分析:(1)配制溶液需要的仪器有:天平、量筒、烧杯、玻璃棒、胶头滴管和100mL容量瓶。
(2)要配制1mol/L的Na2CO3溶液100mL,需要Na2CO3为1mol/L×0.1L×106g/mol=10.6g,弱称量时物码放反了,则质量少了两个游码的质量,所以实际称量的质量为10.6-2×0.6=9.4g。
(3)根据c=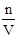 可知,称量的Na2CO3固体中有杂质,溶质的质量比正常值小,所以偏低,溶解Na2CO3固体时溶液溅出少量,溶质的质量比正常值小,所以偏低,没有洗涤烧杯及玻璃棒溶质的质量比正常值小,所以偏低,定容时发现液面高于刻度线,用胶头滴管吸出多余的溶剂,溶液的体积比正常值大,所以偏低,定容时仰视刻度线,溶液的体积比正常值大,所以偏低,定容时俯视刻度线,溶液的体积比正常值小,所以偏高,定容摇匀后,发现液面低于刻度线,再加至刻度线,溶液的体积比正常值大,所以偏低。
可知,称量的Na2CO3固体中有杂质,溶质的质量比正常值小,所以偏低,溶解Na2CO3固体时溶液溅出少量,溶质的质量比正常值小,所以偏低,没有洗涤烧杯及玻璃棒溶质的质量比正常值小,所以偏低,定容时发现液面高于刻度线,用胶头滴管吸出多余的溶剂,溶液的体积比正常值大,所以偏低,定容时仰视刻度线,溶液的体积比正常值大,所以偏低,定容时俯视刻度线,溶液的体积比正常值小,所以偏高,定容摇匀后,发现液面低于刻度线,再加至刻度线,溶液的体积比正常值大,所以偏低。
(4)Na2CO3溶液20ml,则Na2CO3为0.02mol,所以产生CO2为0.02mol,体积为0.448L。将CO2通入到澄清石灰水中产生0.02mol的CaCO3沉淀,质量为2g。
考点:一定物质的量浓度溶液的配制
点评:本题非常简单基础,主要考查学生的基础知识。

用Na2CO3固体配制1mol/L的Na2CO3溶液100mL。
(1)供选用的仪器有:①玻璃棒;②胶头滴管;③酒精灯;④100mL容量瓶;⑤250mL量筒;⑥天平;⑦50mL烧杯;应选用的仪器(填编号) 。
(2)应称取Na2CO3的质量为 g;若称量时砝码和物品放反了,则实际称量的Na2CO3的质量为 g 。
(3)下列操作,会引起所配溶液浓度偏高的是( )
| A.称取的Na2CO3固体中有杂质 |
| B.溶解Na2CO3固体时,因搅拌剧烈使烧杯中的溶液溅出少量 |
| C.没有洗涤烧杯及玻璃棒 |
| D.定容时发现液面高于刻度线,用胶头滴管吸出多余的溶剂 |
F、定容时俯视刻度线
G、定容摇匀后,发现液面低于刻度线,再加至刻度线
(4)取所配Na2CO3溶液20ml,向其中滴加足量的稀盐酸,可得到标况下的气体 L,将得到的气体全部通入足量的澄清石灰水,充分反应后,将沉淀过滤,洗涤,干燥,最后可得固体 g。