题目内容
某有机物A只含有一个氧原子.将0.1mol A在足量氧气中完全燃烧产生3.6g水,产物还能与100mL 2mol/L 烧碱溶液恰好完全反应,将所得溶液在低温下蒸干,能得到16.8g纯净物.请计算:
①A的分子式;
②若A的核磁共振氢谱只有一个吸收峰,请写出A的结构简式.
①A的分子式;
②若A的核磁共振氢谱只有一个吸收峰,请写出A的结构简式.
分析:(1)通过讨论判断出0.1molA完全燃烧生成的二氧化碳的物质的量,从而确定A分子中含有的C,根据生成水的质量确定A中含有的氢原子数目,然后得出的分子式;
(2)A的核磁共振氢谱只有一个吸收峰,说明A分子中含有的4g氢原子所在位置相同,据此判断A的结构,形成A的结构简式.
(2)A的核磁共振氢谱只有一个吸收峰,说明A分子中含有的4g氢原子所在位置相同,据此判断A的结构,形成A的结构简式.
解答:解:(1)0.1mol A完全燃烧生成水的物质的量为:n(H2O)=0.2 mol,所以A中含有4个H,
100mL 2mol/L 烧碱溶液中含有氢氧化钠的物质的量为:n(NaOH)=2mol/L×0.1L=0.2mol,
若纯净物是Na2CO3,则:
CO2+2NaOH=Na2CO3+H2O
1 2
0.2mol 0.1mol
m(Na2CO3)=106g/mol×0.1mol=10.6g<16.8g
若纯净物为碳酸氢钠,则:
CO2 +NaOH=NaHCO3
1 1
0.2mol 0.2mol
m(NaHCO3)=84g/mol×0.2mol=16.8g,
所得纯净物是NaHCO3,n(CO2 )=0.2mol,
所以A分子中含有2个C,4个H,一个O,
所以A的分子式为:C2H4O,
答:A的分子式C2H4O;
(2)由于A的核磁共振氢谱只有一个吸收峰,所以A中的4个氢原子位置相同,
故A的结构简式为: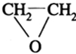 ;
;
答:A的结构简式为 .
.
100mL 2mol/L 烧碱溶液中含有氢氧化钠的物质的量为:n(NaOH)=2mol/L×0.1L=0.2mol,
若纯净物是Na2CO3,则:
CO2+2NaOH=Na2CO3+H2O
1 2
0.2mol 0.1mol
m(Na2CO3)=106g/mol×0.1mol=10.6g<16.8g
若纯净物为碳酸氢钠,则:
CO2 +NaOH=NaHCO3
1 1
0.2mol 0.2mol
m(NaHCO3)=84g/mol×0.2mol=16.8g,
所得纯净物是NaHCO3,n(CO2 )=0.2mol,
所以A分子中含有2个C,4个H,一个O,
所以A的分子式为:C2H4O,
答:A的分子式C2H4O;
(2)由于A的核磁共振氢谱只有一个吸收峰,所以A中的4个氢原子位置相同,
故A的结构简式为:
 ;
;答:A的结构简式为
 .
.点评:本题考查了有机物分子式、结构简式的确定,题目难度中等,注意明确根据燃烧产物判断有机物中含有的C、H原子个数的方法,本题中讨论二氧化碳与氢氧化钠反应产物是解题难点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目


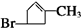
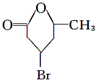
 )是否具有光学活性
)是否具有光学活性






