题目内容
(12分)下表列出前20号元素中的某些元素性质的一些数据:
试回答下列问题:
(1)已知H为Na元素,则以上10种元素中第一电离能最小的是: (写元素符号)。比元素B原子序数大10的元素其基态原子的核外电子排布式是 。
(2)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子。其一分子中共形
成 个σ键, 个π键。
(3) 短周期某主族元素K的电离能情况如图(A)所示。则K元素位于周期表的第 族。
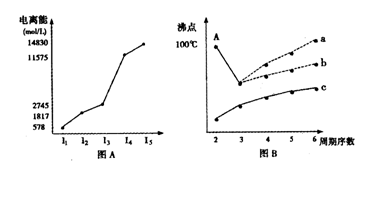
图B是研究部分元素的氢化物的沸点变化规律的图像,折线c可以表达出第 族元素氢化物的沸点的变化规律。
不同同学对某主族元素的氢化物的沸点的变化趋势画出了两条折线—折线a和折线b,你认为正确的是 ,理由是
| 元素 性质 | A | B | C | D | E | F | G | H | I | J |
| 原子半径(10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | — | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | — | -2 | — | -4 | -3 | -1 | — | -3 | -4 |
(1)已知H为Na元素,则以上10种元素中第一电离能最小的是: (写元素符号)。比元素B原子序数大10的元素其基态原子的核外电子排布式是 。
(2)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子。其一分子中共形
成 个σ键, 个π键。
(3) 短周期某主族元素K的电离能情况如图(A)所示。则K元素位于周期表的第 族。

图B是研究部分元素的氢化物的沸点变化规律的图像,折线c可以表达出第 族元素氢化物的沸点的变化规律。
不同同学对某主族元素的氢化物的沸点的变化趋势画出了两条折线—折线a和折线b,你认为正确的是 ,理由是
(12分)(1)K (2分) 1s 22s 22P 63s 23P 63d 104s1或[Ar] 3d104s1 (2分) (3) 7 1 (各1分) (4) IIIA (2分) IVA(2分) ;
b (1分) A点所示的氢化物是水,其沸点在氧族元素的氢化物中最高是由于在水分子间存在着氢键,其强度远大于分子间作用力。(1分)
b (1分) A点所示的氢化物是水,其沸点在氧族元素的氢化物中最高是由于在水分子间存在着氢键,其强度远大于分子间作用力。(1分)
略

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
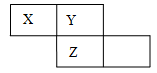
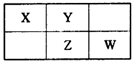
 硅、含量最高的金属是铝
硅、含量最高的金属是铝 电子的都是金属元素
电子的都是金属元素