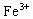题目内容
把铜粉和铁粉的混合物,放入一定量的稀硝酸中,微热,反应完毕发现铜有剩余,则溶液中含有的阳离子是
- A.Cu2+、Fe2+
- B.Cu2+、Fe2+、Fe3+
- C.Cu2+、Fe3+
- D.Fe3+
A
铜有剩余,说明硝酸已经反应完,可能发生的反应有:
Fe+4H++NO3-===Fe3++NO↑+2H2O
3Cu+8H++2NO3-===3Cu2++2NO↑+4H2O
Fe+2Fe3+===3Fe2+
Cu+2Fe3+===2Fe2++Cu2+
从反应可知,当铜有剩余,溶液中Fe3+已消耗尽,铜跟Fe2+不能反应,所以溶液中的阳离子有Cu2+、Fe2+,选A。
铜有剩余,说明硝酸已经反应完,可能发生的反应有:
Fe+4H++NO3-===Fe3++NO↑+2H2O
3Cu+8H++2NO3-===3Cu2++2NO↑+4H2O
Fe+2Fe3+===3Fe2+
Cu+2Fe3+===2Fe2++Cu2+
从反应可知,当铜有剩余,溶液中Fe3+已消耗尽,铜跟Fe2+不能反应,所以溶液中的阳离子有Cu2+、Fe2+,选A。

练习册系列答案
相关题目