题目内容
海带中含碘元素,有人设计如下步骤来提取碘:①加入6%H2O2溶液;②将海带烧成灰,向灰中加入蒸馏水;③加入CCl4振荡;④过滤;⑤用分液漏斗分液;⑥加热煮沸1~2分钟,合理的操作顺序为
| A.②一⑥一④一①一③一⑤ | B.②一①一⑥一③一④一⑤ |
| C.②一①一③一⑥一⑤一④ | D.②一③一①一⑥一⑤一④ |
A
解析试题分析:海水中碘元素以碘离子的形式存在,先灼烧、溶解、过滤除去难溶物,再加氧化剂得到碘单质,最后根据溶解性萃取。答案为A。
考点:考查物质的制备和分离。

练习册系列答案
 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
下列实验方法正确且能达到目的的是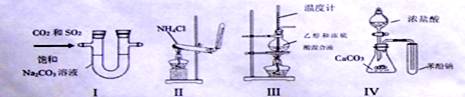
| A.用装置I除去CO2中的SO2 | B.实验室用装置II制备NH3 |
| C.用装置III制备乙烯 | D.装置IV比较酸性H2CO3>苯酚 |
下列四组实验,根据实验事实得出的结论,正确的是
| A.在某试液中滴加BaCl2溶液得白色沉淀,取该白色沉淀加稀盐酸不溶解——原未知试液中一定含有SO42- |
| B.在某未知试液中加入浓的NaOH溶液并加热,产生能使湿润的红色石蕊试纸变蓝的气体——原未知试液中一定含有NH4+ |
| C.在某未知试液中滴加盐酸产生无色气体,将该气体通入足量澄清石灰水中得白色沉淀——原未知试液中一定含有CO32- |
| D.用洁净的铂丝蘸取未知物质,放在无色火焰上灼烧,其焰色为黄色——该未知物中一定只含钠元素 |
下列阳离子中,不能用于区别SO42—、OH—两种离子的是
| A.Fe3+ | B.Ba2+ | C.Cu2+ | D.H+ |
下列有关物质检验的实验结论正确的是
| | 操作 | 现象 | 结论 |
| A. | 向某溶液中滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| B. | 向某无色溶液中滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| C. | 用洁净铂丝蘸取某溶液进行焰色反应 | 火焰呈黄色 | 溶液中有K+ |
| D. | 将某气体通入品红溶液中 | 品红溶液褪色 | 该气体一定是SO2 |
检验下列物质中是否含有杂质(括号内为杂质),检验方法及除杂试剂均正确的是( )
| 物质及其杂质 | 检验 | 除杂 |
| A.Cl2(HCl) | 湿润的淀粉KI试纸 | 饱和食盐水 |
| B.NaHCO3溶液(Na2CO3) | Ca(OH)2溶液 | 过量CO2 |
| C.CO2(HCl) | AgNO3溶液(含稀硝酸) | 饱和Na2CO3溶液 |
| D.NO(NO2) | 观察颜色或湿润的淀粉KI试纸 | 水 |
下列有关实验原理、方法、操作或结论不正确的是( )
| A.除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶 |
| B.用水湿润pH试纸测量某溶液的pH,一定会产生实验误差 |
| C.容量瓶和锥形瓶用蒸馏水洗净后即可使用,滴定管用蒸馏水洗净后,必须用所盛溶液润洗几次后方可使用 |
| D.称取a克Na2CO3和NaHCO3混合物充分加热,减重b克,可测定混合物中Na2CO3的质量分数 |
下列对Ⅰ~Ⅳ实验的现象预测正确的是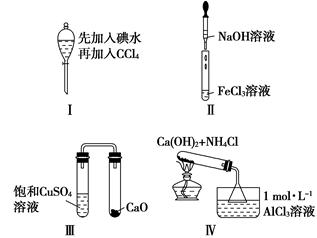
| A.实验Ⅰ:振荡后静置,液体分层,下层液体无色 |
| B.实验Ⅱ:滴入氢氧化钠溶液后,试管中出现白色沉淀迅速变为灰绿色最后变为红褐色 |
| C.实验Ⅲ:一段时间后,饱和CuSO4溶液中出现蓝色晶体 |
| D.实验Ⅳ:加热后,水槽中先生成白色沉淀,后逐渐溶解 |
按以下实验方案可以从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。
下列说法错误的是 ( )。
| A.步骤(1)需要过滤装置 |
| B.步骤(2)需要用到分液漏斗 |
| C.步骤(3)需要用到坩埚 |
| D.步骤(4)需要蒸馏装置 |