题目内容
向2L密闭容器中通入a mol气体A和b mol气体B,在一定条件下发生反应:
xA(g)+yB(g)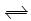 pC(g)+qD(g) 已知:平均反应速率
pC(g)+qD(g) 已知:平均反应速率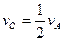 ;反应2 min时A的浓度减少了a/6 mol/L,B的物质的量减少了
;反应2 min时A的浓度减少了a/6 mol/L,B的物质的量减少了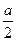 mol,有a mol D生成。
mol,有a mol D生成。
回答下列问题:
(1)反应2 min内,VA= ,vB=
(2)化学方程式中,x= y= p= q=
(3)反应达到平衡时,D为2a mol,则B的转化率为
(4)如果只升高反应温度,其他反应条件不变,平衡时D为1. 5a mol则该反应的
△H 0;(填“>、<或-”)
(5)如果其他条件不变,将容器的容积变为1L,进行同样的实验,则与上述反应比较:①反应速率 (填:“增大”“减小或“不变”)。理由是_
②平衡时反应物的转化率 (填:“增大”“减小”或“不变”)理由是
(1)a/12 mol/L·min a/8 mol/L·min
(2)2 3 1 6
(3)a/b × 100%
(4)<
(5)①增大; 体积减小,反应物的浓度增大,因而使反应速率增大。
②减小; 体积减小,气体的压强增大,平衡向气体分子数少的方向(即逆反应方向)移动,因而反应物转化率减小。
解析

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目


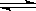 2NH3(g);已知:反应2min达到平衡 ,此时N2的浓度减少了2/3。
2NH3(g);已知:反应2min达到平衡 ,此时N2的浓度减少了2/3。