题目内容
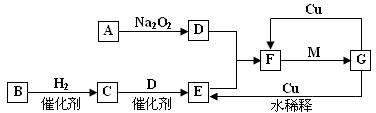
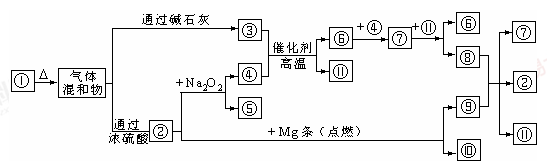
下图表示由短周期元素组成的一些物质之间的转化关系(某些反应产物已略去)。各方框表示有关的一种反应物或生成物(某些物质已经略去),其中A、B、D在常温下均为无色无刺激性气味的气体,C是使湿润的红色石蕊试纸变蓝的气体,M是最常见的无色液体。
⑴ 物质F的化学式 。
⑵ 物质B的电子式 。
⑶ 写出C→E的化学方程式 。
⑷ 写出G→E的离子方程式 。

⑴ 物质F的化学式 。
⑵ 物质B的电子式 。
⑶ 写出C→E的化学方程式 。
⑷ 写出G→E的离子方程式 。
(1)NO2
(2)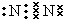
(3)4NH3 + 5 O2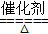 4NO + 6H2O
4NO + 6H2O
(4)3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
(2)
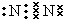
(3)4NH3 + 5 O2
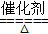 4NO + 6H2O
4NO + 6H2O(4)3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
试题分析:C是使湿润的红色石蕊试纸变蓝的气体,应为NH3,则B为N2,E为NO,G为HNO3,F为NO2,M是最常见的无色液体,应为H2O,A为可与过氧化钠反应的气体,应为CO2,则
(1)由以上分析可知F为NO2,故答案为:NO2;
(2)由以上分析可知B为N2,电子式为
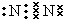 ,故答案为:
,故答案为: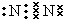 ;
;(3)C为NH3,在催化作用下与氧气反应可生成NO,为工业制硝酸的重要反应,反应的化学方程式为4NH3 + 5 O2
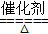 4NO + 6H2O,故答案为4NH3 + 5 O2
4NO + 6H2O,故答案为4NH3 + 5 O2 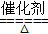 4NO + 6H2O。
4NO + 6H2O。(4)G为HNO3,加水稀释成稀硝酸,可与铜反应生成NO,反应的化学方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,故答案为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。

练习册系列答案
 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目


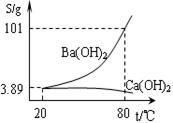
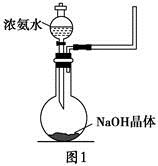

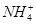 +OH-,NaOH晶体使该可逆反应的平衡向左移动
+OH-,NaOH晶体使该可逆反应的平衡向左移动