题目内容
【题目】下列化学用语正确的是
A. NaHCO3的水解方程式:HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
B. 醋酸铵的电离:CH3COONH4![]() CH3COO-+NH4+
CH3COO-+NH4+
C. 氯化银的溶解平衡表达式:AgCl(s) ![]() Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)
D. 汽车尾气净化反应2NO+2CO=2CO2+N2能够自发进行,则该反应的△H>0
【答案】C
【解析】A. NaHCO3的水解方程式:HCO3-+H2O![]() OH-+H2CO3,A错误;B. 醋酸铵是强电解质,电离方程式为:CH3COONH4=CH3COO-+NH4+,B错误;C. 氯化银的溶解平衡表达式:AgCl(s)
OH-+H2CO3,A错误;B. 醋酸铵是强电解质,电离方程式为:CH3COONH4=CH3COO-+NH4+,B错误;C. 氯化银的溶解平衡表达式:AgCl(s)![]() Ag+(aq)+Cl-(aq),C正确;D. 汽车尾气净化反应2NO+2CO=2CO2+N2能够自发进行,由于△S<0,则根据△G=△H-T△S<0可知该反应的△H<0,D错误,答案选C。
Ag+(aq)+Cl-(aq),C正确;D. 汽车尾气净化反应2NO+2CO=2CO2+N2能够自发进行,由于△S<0,则根据△G=△H-T△S<0可知该反应的△H<0,D错误,答案选C。

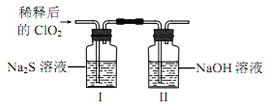
【题目】二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为11℃,可用于处理含硫废水。某小组在实验室中探究ClO2与Na2S的反应。回答下列问题:
(l)ClO2的制备:(已知:SO2+2NaClO3+H2SO4=2ClO2↑+2NaHSO4)

①装置A中反应的化学方程式为_______________。
②欲收集干燥的ClO2,选择上图中的装置,其连接顺序为 a→_________(按气流方向,用小写字母表示)
③装置D的作用是_________。
(2)ClO2与 Na2S 的反应
将上述收集到的ClO2用 N2稀释以增强其稳定性,并将适量的稀释后的ClO2通入上图所示装置中充分反应,得到无色澄清溶液。一段时间后,通过下列实验探究 I 中反应的产物。
操作步骤 | 实验现象 | 结论 |
取少量Ⅰ中溶液于试管甲中, 加入Ba(OH)2溶液,振荡 | ①_________ | 有硫酸根离子生成 |
另取少量Ⅰ中溶液于试管乙中, 滴加品红溶液和盐酸 | 品红溶液不翅色 | ② 无_____生成 |
若在试管甲中继续加Ba(OH)2溶液至 过量,静置,取上层清液于试管丙③______ | 有白色沉淀生成 | 有Cl-生成 |
④ClO2与Na2S反应的离子方程式为__________。用于处理含硫废水时,ClO2相对于Cl2的优点是____________(任写2条)。
【题目】Ca3N2某实验小组利用如下装置(部分固定装置略)进行氮气与钙的反应,并探究其产物的性质及化学式。请回答下列问题。

(1)仪器B的名称是_____________,B中固体物质为_______________。
(2)反应过程中末端导管必须插入试管C的水中,目的是______。(填字母)
A.吸收反应中剩余的氮气
B.控制通入气体的流速
C.防止空气中的氧气倒流进入反应装置,干扰反应
(3)将制备氮化钙的操作步骤补充完整:
①打开活塞K并通入N2;
②点燃酒精灯,进行反应;
③反应结束后,__________________。
(4)该小组同学认为根据相应的质量关系可以求出生成物的化学式,数据记录如下:
A的质量m0/g | A与钙的质量m1/g | A与产物的质量m2/g |
14.80 | 15.08 | 15.15 |
①通过计算得到化学式CaxN2,其中x=______。
②小组同学查阅资料得知产物为Ca3N2,能与水强烈反应,请写出Ca3N2与水反应的化学方程式_________________,设计实验检验Ca3N2与水反应产物的操作及现象__________________。
