题目内容
常温下,一种烷烃A和一种烯烃B组成的混合气体。A和B分子最多只含有4个碳原子,且B分子的碳原子数比A分子的多。
(1)将1 L该混合气体充分燃烧,在同温、同压下得到2.5 L CO2气体。试推断原混合气体中A和B所有可能的组合及其体积比,并将结论填入下表。
| 组合编号 | A的分子式 | B的分子式 | A和B的体积比V(A)∶V(B) |
(2)120 ℃时取1 L该混合气体与9 L O2混合,充分燃烧,当恢复到120 ℃和燃烧前的压强时,体积增大6.25%。试通过计算确定A和B的分子式。
(1)
| 组合编号 | A的分子式 | B的分子式 | A和B的体积比(VA∶VB) |
| ① | CH4 | C3H6 | 1∶3 |
| ② | CH4 | C4H8 | 1∶1 |
| ③ | C2H6 | C3H6 | 1∶1 |
| ④ | C2H6 | C4H8 | 3∶1 |
(2)A:C2H6 B:C4H8
解析:
(1)据题意知:混合气体的平均组成中碳原子个数为2∶5,则A分子中碳原子个数小于2.5,B分子碳原子个数大于2.5。
(2)设混合气体的平均分子式为C2.5Hx,则根据
C2.5Hx+(2.5+![]() )O2
)O2![]() 2.5CO2+
2.5CO2+![]() H2O Δn
H2O Δn
1 2.5+![]() 2.5x
2.5x ![]()
![]() -1
-1
1 0.625
有: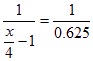 ,x=6.5,故只有C2H6与C4H8符合。
,x=6.5,故只有C2H6与C4H8符合。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案| A、CH4、C3H6 | B、C2H6、C3H6 | C、CH4、C4H8 | D、C2H6、C4H8 |
常温下,一种烷烃A和一种烯烃B组成混合气体,A、B分子最多只含4个碳原子,且B分子的碳原子数比A分子的多。将1L该混合气体充分燃烧,在同温同压下得到2.5LCO2气体,试推断混合气体中A和B所有可能的组合及其体积比,并将结果填如下表:
| 组合编号 | A的分子式 | B的分子式 | A和B是体积比 (VA:VB) |
| ① | |||
| ② | |||
| ③ | |||
| ④ |
常温下,一种烷烃A和一种单烯烃B组成混合气体,A或B分子中最多只含有4个碳原子,且B分子的碳原子数比A分子的多。
⑴将1L该混合气体充分燃烧,在同温同压下得到2.5LCO2气体。试推断原混合气体中A和B所有可能的组合及其体积比,并将结果填入下表:
| 组合编号 | A的分子式 | B的分子式 | A、B的体积比 |
| ① | |||
| ② | |||
| ③ | |||
| ④ |
⑵120℃时取1L该混合气体与9LO2混合,充分燃烧,当恢复到120℃和原压强时,体积增大6.25%,试通过计算确定A、B的分子式。