题目内容
硫酸氢钠(NaHSO4)在水溶液中可以完全电离为Na+和HSO ,HSO
,HSO 在较稀(如1 mol·L-1以下)的溶液中,可完全电离为H+和SO
在较稀(如1 mol·L-1以下)的溶液中,可完全电离为H+和SO 。不过,在浓度大的溶液中HSO
。不过,在浓度大的溶液中HSO 不能完全电离,而是与H+、SO
不能完全电离,而是与H+、SO 共同存在于同一溶液中。
共同存在于同一溶液中。
(1)硫酸氢钠(NaHSO4)所属的物质类别是( )
(2)NaHSO4溶液的pH 7。(填“>”“<”或“=”=
(3)在稀NaHSO4溶液中加入Na2CO3溶液时,可以得到无色、无味的气体,该气体可以使澄清石灰水变浑浊。写出稀NaHSO4溶液与Na2CO3溶液反应的化学方程式和离子方程式。
 ,HSO
,HSO 在较稀(如1 mol·L-1以下)的溶液中,可完全电离为H+和SO
在较稀(如1 mol·L-1以下)的溶液中,可完全电离为H+和SO 。不过,在浓度大的溶液中HSO
。不过,在浓度大的溶液中HSO 不能完全电离,而是与H+、SO
不能完全电离,而是与H+、SO 共同存在于同一溶液中。
共同存在于同一溶液中。(1)硫酸氢钠(NaHSO4)所属的物质类别是( )
| A.酸 | B.盐 | C.碱 | D.氧化物 |
(3)在稀NaHSO4溶液中加入Na2CO3溶液时,可以得到无色、无味的气体,该气体可以使澄清石灰水变浑浊。写出稀NaHSO4溶液与Na2CO3溶液反应的化学方程式和离子方程式。
(1)B (2)<
(3)2NaHSO4+Na2CO3 2Na2SO4+H2O+CO2↑
2Na2SO4+H2O+CO2↑
2H++CO
 H2O+CO2↑
H2O+CO2↑
(3)2NaHSO4+Na2CO3
 2Na2SO4+H2O+CO2↑
2Na2SO4+H2O+CO2↑2H++CO

 H2O+CO2↑
H2O+CO2↑HSO 可以看成H2SO4电离产生的一种酸根离子,这样硫酸氢钠可看成是由金属阳离子Na+与酸根阴离子HSO
可以看成H2SO4电离产生的一种酸根离子,这样硫酸氢钠可看成是由金属阳离子Na+与酸根阴离子HSO 组成的,因而它是一种盐。由于硫酸氢钠电离出的阳离子并不都是H+,因此它既不属于酸也不属于一般的盐,而是一种酸式盐。
组成的,因而它是一种盐。由于硫酸氢钠电离出的阳离子并不都是H+,因此它既不属于酸也不属于一般的盐,而是一种酸式盐。
由于HSO 电离可以产生H+,故其水溶液应该显酸性,其pH<7。
电离可以产生H+,故其水溶液应该显酸性,其pH<7。
稀NaHSO4溶液与Na2CO3溶液反应得到的无色、无味、可使澄清石灰水变浑浊的气体应该是二氧化碳。HSO 在稀溶液里完全电离为H+和SO
在稀溶液里完全电离为H+和SO ,则NaHSO4溶液与Na2CO3溶液的反应实质上就是H+与CO
,则NaHSO4溶液与Na2CO3溶液的反应实质上就是H+与CO 的反应。
的反应。
 可以看成H2SO4电离产生的一种酸根离子,这样硫酸氢钠可看成是由金属阳离子Na+与酸根阴离子HSO
可以看成H2SO4电离产生的一种酸根离子,这样硫酸氢钠可看成是由金属阳离子Na+与酸根阴离子HSO 组成的,因而它是一种盐。由于硫酸氢钠电离出的阳离子并不都是H+,因此它既不属于酸也不属于一般的盐,而是一种酸式盐。
组成的,因而它是一种盐。由于硫酸氢钠电离出的阳离子并不都是H+,因此它既不属于酸也不属于一般的盐,而是一种酸式盐。由于HSO
 电离可以产生H+,故其水溶液应该显酸性,其pH<7。
电离可以产生H+,故其水溶液应该显酸性,其pH<7。稀NaHSO4溶液与Na2CO3溶液反应得到的无色、无味、可使澄清石灰水变浑浊的气体应该是二氧化碳。HSO
 在稀溶液里完全电离为H+和SO
在稀溶液里完全电离为H+和SO ,则NaHSO4溶液与Na2CO3溶液的反应实质上就是H+与CO
,则NaHSO4溶液与Na2CO3溶液的反应实质上就是H+与CO 的反应。
的反应。
练习册系列答案
相关题目
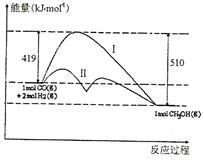 反应CO(g)+2H2(g)
反应CO(g)+2H2(g)  CH3OH(g)过程中的能量变化 情况如右图所示,曲线I和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是
CH3OH(g)过程中的能量变化 情况如右图所示,曲线I和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是  、H
、H 、Cr(OH)
、Cr(OH) 、H
、H O
O +OH-====NH3·H2O
+OH-====NH3·H2O +5H+====Al(OH)3↓+Al3++H2O
+5H+====Al(OH)3↓+Al3++H2O