题目内容
红磷(P)和Cl2发生反应生成PCl3和PCl5,反应过程和能量的关系如下图所示,图中的ΔH表示生成1 mol产物的数据。已知PCl5分解生成PCl3和Cl2,该分解反应是可逆反应。下列说法正确的是( )

A.其他条件不变,降低温度有利于PCl5的生成
B.反应2P(s)+5Cl2(g)===2PCl5(g)对应的反应热 ΔH=-798 kJ/mol
C.P和Cl2反应生成PCl3的热化学方程式为:2P(s)+3Cl2(g)===2PCl3(g) ΔH=-306 kJ/mol
D.其他条件不变,对于2PCl5(g)===2P(s)+5Cl2(g) ΔH反应,增大压强,PCl5的转化率减小,ΔH减小
解析:选AB 由图可知,P和Cl2反应生成PCl5的热化学方程式是:P(s)+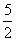 Cl2(g)===PCl5(g) ΔH=-399 kJ/mol,A项正确,B项正确;图中的ΔH表示生成1 mol产物的数据,C项错误;热化学方程式不变,ΔH不变,D项错误。
Cl2(g)===PCl5(g) ΔH=-399 kJ/mol,A项正确,B项正确;图中的ΔH表示生成1 mol产物的数据,C项错误;热化学方程式不变,ΔH不变,D项错误。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列设备工作时,将化学能转化为热能的是( )
| A | B | C | D |
|
|
|
|
|
| 硅太阳能电池 | 锂离子电池 | 太阳能集热器 | 燃气灶 |
 与Cl2反应的产物之一为SO
与Cl2反应的产物之一为SO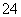 。下列说法中,错误的是( )
。下列说法中,错误的是( ) 可脱去2 mol Cl2
可脱去2 mol Cl2 接钢轨,请写出反应的化学方程式:________________________________________________________________________。
接钢轨,请写出反应的化学方程式:________________________________________________________________________。 ___________________________________________________
___________________________________________________ _______________________________________。
_______________________________________。



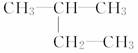 ______________________________________________;
______________________________________________;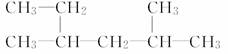 ___________________________________;
___________________________________;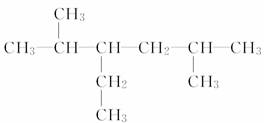 _______________________________;
_______________________________;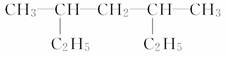 ___________________________________;
___________________________________; __________________________。
__________________________。
 4NO+6H2O
4NO+6H2O 2C
2C 3(g);△H=-Q1 kJ/mol(Q1>0), 在一个有催化剂的固定容积的容器中加入2 molA2和1 molB2,在500℃时充分反应,达平衡后C3的浓度为w mol·L-1,放出热量为Q2 kJ。
3(g);△H=-Q1 kJ/mol(Q1>0), 在一个有催化剂的固定容积的容器中加入2 molA2和1 molB2,在500℃时充分反应,达平衡后C3的浓度为w mol·L-1,放出热量为Q2 kJ。 A2的转化率为________。
A2的转化率为________。 之间满足何种关系
之间满足何种关系 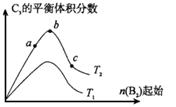 c.2v逆(A2)=v正(B2) d.容器内的密度保持不变
c.2v逆(A2)=v正(B2) d.容器内的密度保持不变 .增大压强 c.及时分离生成的C3 d.升高温度
.增大压强 c.及时分离生成的C3 d.升高温度