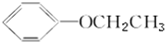题目内容
用浓硫酸吸收SO3可得发烟硫酸(H2SO4?SO3).某化工厂用1.5m3 98.3%的浓硫酸(密度为1.84g/mL)吸收SO3形成发烟硫酸,再与水混合,可得到95%的硫酸(密度为1.79g/mL) m3(保留2位小数).
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:先根据浓硫酸的体积、质量分数、密度计算出含有的硫酸、水的物质的量,从而计算出发烟硫酸的物质的量,然后设与水混合后的硫酸溶液的体积为VmL,根据稀释过程中硫酸的质量不变计算出V,再将计算结果转换成单位为m3的硫酸体积即可.
解答:
解:1.5m3 98.3%的浓硫酸(密度为1.84g/mL)中含有硫酸的质量为:m(H2SO4)=1.5×106mL×1.84g/mL×98.3%≈2.713×106g,硫酸的物质的量为:
≈2.769×104mol,
1.5m3 98.3%的浓硫酸(密度为1.84g/mL)中含有水的质量为:1.5×106mL×1.84g/mL×(1-98.3%)=4.692×104g,水的物质的量为:
≈2.607×103mol,水与三氧化硫反应生成硫酸的物质的量等于水的物质的量,
所以用水吸收后形成发烟硫酸的物质的量为:2.769×104mol+2.607×103mol=3.0297×104mol,
用水稀释后的溶液中含有硫酸的物质的量为:2×3.0297×104mol=6.0294×104mol,
设稀释后溶液的体积为VmL,则:VmL×1.79g/mL×95%=6.0294×105mol×98g/mol,
解得:V≈3.49×106mL=3.49m3,
故答案为:3.49.
| 2.713×106g |
| 98g/mol |
1.5m3 98.3%的浓硫酸(密度为1.84g/mL)中含有水的质量为:1.5×106mL×1.84g/mL×(1-98.3%)=4.692×104g,水的物质的量为:
| 4.692×104g |
| 18g/mol |
所以用水吸收后形成发烟硫酸的物质的量为:2.769×104mol+2.607×103mol=3.0297×104mol,
用水稀释后的溶液中含有硫酸的物质的量为:2×3.0297×104mol=6.0294×104mol,
设稀释后溶液的体积为VmL,则:VmL×1.79g/mL×95%=6.0294×105mol×98g/mol,
解得:V≈3.49×106mL=3.49m3,
故答案为:3.49.
点评:本题考查了有关物质的量的计算,题目难度中等,注意掌握浓硫酸的水能够与三氧化硫反应生成硫酸,计算发烟硫酸的物质的量时不能漏掉浓硫酸与水反应生成的硫酸的物质的量.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、Na2CO3溶液:c(OH-)+c(H+)=c(HCO3-)+2c(H2CO3) |
| B、某二元酸(用H2A表示)在水中的电离方程式是:H2A═H++HA-,HA-?H++A2-则NaHA溶液中:c(Na+)=c(A2-)+c(HA-)+c(H2A) |
| C、常温下,pH=12的氨水溶液与pH=2的盐酸溶液等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D、常温下,10mL pH=12的Ba(OH)2溶液与40mL c mol?L-1的NaHSO4溶液混合,当溶液中的Ba2+、SO42-均恰好完全沉淀,若混合后溶液的体积为50mL,则溶液pH=11 |
下列化学方程式或离子方程式正确的是( )
| A、常温下,将铁片置于浓硝酸中:Fe+6HNO3=Fe(NO3)3+3NO2↑+3H2O |
| B、向浓硝酸中加入铜片:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
| C、向(NH4)2SO4溶液中加入适量Ba(OH)2:Ba2++SO42-=BaSO4↓ |
| D、向浓硫酸中加入少量锌:Zn+2H+=Zn2++H2↑ |
21世纪化学的最新定义为“化学是一门创造新物质的科学”.下列有关说法不正确的是( )
| A、利用人工光合成反应,探究将二氧化碳转化为碳氢化合物作燃料,属于低碳技术 |
| B、开发安全、高效、低毒及低残留的新型农药 |
| C、大量生产聚乙烯、聚氯乙烯一次性超薄袋,方便日常生活 |
| D、制备物质时探究化学反应中高的选择性、转化率和原子利用率,属于“绿色”的生产工艺 |
常温下,下列各组离子在指定的溶液中可能大量共存的是( )
| A、无色透明溶液中:Al3+、Ca2+、Cl-、HCO3- |
| B、含大量Fe3+的溶液中:K+、I-、SO42-、NO3- |
| C、与Al反应放出H2的溶液中:NH4+、Na+、NO3-、F- |
| D、由水电离出的c(H+)=1.0×10-14mol/L的溶液中:Mg2+、K+、Cl-、SO42- |


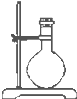


 ,分析该物质结构,回答问题:
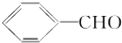
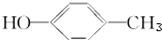
,分析该物质结构,回答问题: 的物质互为同分异构体的是( )
的物质互为同分异构体的是( )