��Ŀ����
����Ŀ����ͼ���ɳ���Ԫ����ɵ�һЩ���ʼ��仯����֮���ת����ϵͼ�����³�ѹ�£�B��E��F��H��I��Ϊ����,F��ɫ��ζ������ʹ����ʯ��ˮ���ʴ��B��E��I���д̼�����ζ��E��ʹʪ��ĺ�ɫʯ����ֽ������B��E�ڿ�����������������̣�IΪ����ɫ��A��һ�ֳ����ĵ��ʣ�FҲ������ֱ�ӷֽ�ɵõ���C��G��K����ɫ��Ӧ�ʻ�ɫ������Ӧ�в��������Z��ȥ��

��ش��������⣺
��1������D�Ļ�ѧʽΪ____________����ˮ��Һ�������ӵļ��鷽��Ϊ(���ֱ���)______��
��2��д����Ӧ�۵Ļ�ѧ����ʽ��__________________��
��3��д����Ӧ�ܵ����ӷ���ʽ��__________________��
��4��д����Ӧ�ݵĻ�ѧ����ʽ��__________________��
���𰸡� NH4Cl ��NaOH��Һ�����ȣ�������ʹʪ��ĺ�ɫʯ����ֽ�������������ɣ������Һ�д���NH4+ Na2CO3+CO2+H2O=2NaHCO3 3Cu+8H++2NO3-=3Cu2++2NO��+4H2O 3NO2+H2O=2HNO3+NO
�����������������F��ɫ��ζ������ʹ����ʯ��ˮ���ʴ���Ƴ�F��CO2��E��ʹʪ��ĺ�ɫʯ����ֽ������E��NH3��B��E�ڿ�����������������̣�B��HCl�� D��NH4Cl��IΪ����ɫ���壬I��NO2���ɷ�Ӧ�� 3NO2+H2O=HNO3+NO����֪J��HNO3��H��NO��C��G��K����ɫ��Ӧ�ʻ�ɫ��C��G��K������Ԫ�أ�A��һ�ֳ����ĵ��ʣ�A����Σ�C���������ƣ��ɷ�Ӧ����֪A��NH4HCO3�� �ɷ�Ӧ����֪G��Na2CO3��K��NaHCO3�������Ϸ�����֪��1������D�Ļ�ѧʽΪNH4Cl�������Ӧ�ų�������笠����ӵļ��鷽��Ϊ��NaOH��Һ�����ȣ�������ʹʪ��ĺ�ɫʯ����ֽ�������������ɣ������Һ�д���NH4+ ����2��̼���ơ�������̼��ˮ��Ӧ����̼�����ƵĻ�ѧ����ʽΪNa2CO3+CO2+H2O=2NaHCO3����3��������ͭ��Ӧ��������ͭ��һ��������ˮ�����ӷ���ʽΪ3Cu+8H++2NO3-=3Cu2++2NO��+4H2O����4��������������ˮ���������һ�������Ļ�ѧ����ʽΪ3NO2+H2O=2HNO3+NO��

 ������ϵ�д�
������ϵ�д�����Ŀ��
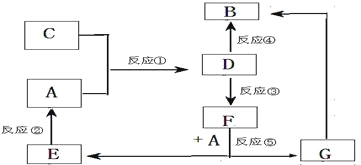
������AΪ�������ʣ� BΪ���ɫ���壻EΪ�ܶ���С�����壻GΪdz��ɫ��Һ��
������DΪ��ɫ��Һ��������������Һ��Ӧ���ɲ�����ϡ����İ�ɫ������
������D�ܽ�ij������������ΪF��F�Ǻ�������Ԫ�صĻ����
��ش��������⣺
��1��������Ӧ�������û���Ӧ���� ������ţ���
��2��G����B�Ĺ����������ֵ����� ��
��Ӧ�������ӷ���ʽ ��
��3��D��ˮ��Һ�����ԣ��������ӷ���ʽ����ԭ�� ��
��4��ʵ������ȡC�Ļ�ѧ����ʽΪ ��
������C��������ʵ�顣��֪������Ӧ�����У�ÿ����0.1mol KI,ת�Ƶĵ�����ԼΪ3.612��1023 �����밴��Ҫ����գ�
ʵ�鲽�� | ʵ������ | �û�ѧ������� |
����������ͨ�����KI��Һ | ��Һ������ ɫ | |
����ͨ������ | ��Һ�����ɫ | |
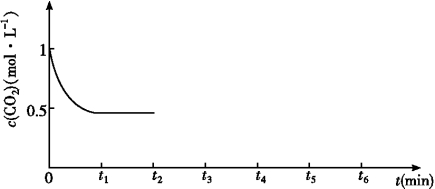
����Ŀ����2L�ܱ�������������0.100molCO�����0.080molCuO���壬800��ʱ�������·�Ӧ��2CuO��s��+CO��g��![]() Cu2O��s��+CO2��g����n��CuO����ʱ��ı仯�����
Cu2O��s��+CO2��g����n��CuO����ʱ��ı仯�����
ʱ����min�� | 0 | 1 | 2 | 3 | 4 | 5 |
n��CuO����mol�� | 0.080 | 0.060 | 0.040 | 0.020 | 0.020 | 0.020 |
��1����CO��ʾǰ2min�ڵĻ�ѧ��Ӧ����=
��2������˷�Ӧ��800Cʱ�Ļ�ѧƽ�ⳣ��k=
��3������ƽ������ϵ�м���CO��CO2��0.05mol�����ʱV������ V������
��4��������ԭCuO��CO������C��ˮ������Ӧ�Ƶá�
��֪��![]() H=-393.5kJ/mol
H=-393.5kJ/mol
![]() H=-566kJ/mol
H=-566kJ/mol
![]() H=-571.6kJ/mol
H=-571.6kJ/mol
��C��s��+H2O��g��![]() CO��g��+H2��g�� H= ��
CO��g��+H2��g�� H= ��