题目内容
【题目】原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。
(1)X元素是____________ ;Y元素在周期表中的位置为____________ 。
(2)X与W组成的化合物电子式为__________________________ 。
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,化学方程式为 ___________________________。
(4)常温下w的一种气态氧化物能与氯水发生氧化还原反应,写出反应的离子方程式____。
(5)由X、Y、Z、W四种元素组成的一种离子化合物A,已知1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体。写出加热条件下A与NaOH溶液反应的离子方程式:__________________。
【答案】H 第二周期VA族 ![]() 3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O H2S+Cl2=S↓+2H++2Cl-
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O H2S+Cl2=S↓+2H++2Cl- ![]()
【解析】
原子序数由小到大排列的四种短周期元素X、Y、Z、W,在周期表中X是原子半径最小的元素,则X为H元素;Z、W位于同主族,设Z的原子序数为x,则W的原子序数为x+8,Y、Z左右相邻,Y的原子序数为x-1,由四种元素的原子序数之和为32,则1+(x-1)+x+(x+8)=32,解得x=8,即Y为N元素,Z为O元素,W为S元素,然后利用元素及其单质、化合物的性质来解答。
(1)由上述分析可知,X元素为H;Y为N元素,其位于元素周期表第二周期VA族,
故答案为:H;第二周期VA族;
(2)H与S组成的化合物为H2S,其电子式为![]() ,
,
故答案为:![]() ;
;
(3)由H、N、O、S中三种元素组成的能够与铜反应的稀强酸为硝酸,其化学方程式为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,
故答案为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O;
(4)常温下,H2S能够与氯水发生氧化还原反应,其离子方程式为:H2S+Cl2=S↓+2H++2Cl-,
故答案为:H2S+Cl2=S↓+2H++2Cl-;
(5)由H、N、O、S组成的离子化合物,1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体,说明1mol该物质中含有2mol铵根离子,由此可知,A为(NH4)2SO4或(NH4)2SO3等,其与NaOH溶液在加热条件下反应的离子方程式为:![]() ,
,
故答案为:![]() 。
。

 阅读快车系列答案
阅读快车系列答案【题目】下列反应中,属于消去反应的是
A.CH2=CH2+HCl 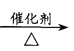 CH3CH2Cl
CH3CH2Cl
B.CH4+Cl2![]() CH3Cl+HCl
CH3Cl+HCl
C.![]() +Br2
+Br2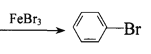 +HBr
+HBr
D.CH3CH2Br+NaOH![]() CH2=CH2+NaBr+H2O
CH2=CH2+NaBr+H2O
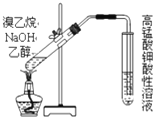
【题目】氯苯在染料、医药工业中有广泛的应用,某实验小组利用如下装置合成氯苯(支撑用的铁架台部分省略)并通过一定操作提纯氯苯。
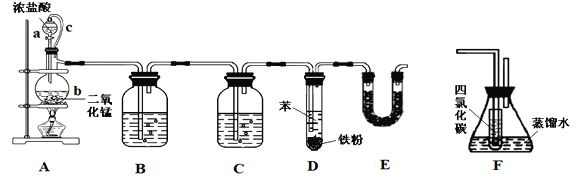
反应物和产物的相关数据列表如下:
密度/g·cm-3 | 沸点/℃ | 水中溶解性 | |
苯 | 0.879 | 80.1 | 微溶 |
氯苯 | 1.11 | 131.7 | 不溶 |
请按要求回答下列问题。
(1)装置A中橡胶管c的作用是______________,装置E的作用是__________________。
(2)实验时;使a中的浓盐酸缓缓滴下,可观察到仪器b内的现象是________________,写出反应的离子方程式______________________________________。
(3)为证明氯气和苯发生的是取代而不是加成反应,该小组用装置F说明,则装置F置于________之间(填字母),F中小试管内CCl4的作用是___________________,还需使用的试剂是______________。
(4)已知D中加入5 mL苯,经过提纯后收集到氯苯3.0 g,则氯苯的产率为_________%(保留三位有效数字)。