题目内容
将过量的气体通入到一种溶液中,一定能产生沉淀的是
①二氧化硫通入到硝酸钡溶液中 ②二氧化碳通入到偏铝酸钠溶液中 ③二氧化碳通入到氯化钙溶液中 ④氨气通入到氯化镁溶液中
①二氧化硫通入到硝酸钡溶液中 ②二氧化碳通入到偏铝酸钠溶液中 ③二氧化碳通入到氯化钙溶液中 ④氨气通入到氯化镁溶液中
| A.只有①②③ | B.只有①② | C.只有②③ | D.只有①②④ |
D
二氧化硫的化学性质;氨的化学性质.
分析:A、依据二氧化硫与水反应生成亚硫酸,在酸性溶液中硝酸根具有强氧化性分析;
B、从碳酸的酸性强于氢氧化铝,氢氧化铝是难溶的沉淀分析;
C、碳酸钙溶于酸中不能存在;
D、从氢氧化铝溶于强酸强碱.不溶于弱酸弱碱分析.
解:①二氧化硫通入到硝酸钡溶液中,二氧化硫与水反应生成亚硫酸,在酸性环境中硝酸根具有强氧化性,把亚硫酸钡氧化为硫酸钡沉淀,故①符合;
②二氧化碳通入到偏铝酸钠溶液中,碳酸酸性强于氢氧化铝,发生反应,CO2+3H2O+2AlO2-=2Al(OH)3↓+CO32-,故②符合;
③二氧化碳通入到氯化钙溶液中,碳酸钙溶于盐酸,所以不发生反应,故③不符合;
④氨气通入到氯化铝溶液中,氢氧化铝不溶于弱碱,发生反应为Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故④符合;
综上所述①②④符合;
故选D.

练习册系列答案
相关题目
 MnCl2+Cl2↑+2H2O ,因此盐酸应当具有的性质是
MnCl2+Cl2↑+2H2O ,因此盐酸应当具有的性质是 二等奖,定名为“84”肝炎洗消液,后更名为“84消毒液”。
二等奖,定名为“84”肝炎洗消液,后更名为“84消毒液”。 学反应方程式_______________________;另外,电解NaCl溶液可直接制备84消毒液,通电时氯气被溶液完全吸收,请写出电解NaCl溶液的化学反应方程式___________。
学反应方程式_______________________;另外,电解NaCl溶液可直接制备84消毒液,通电时氯气被溶液完全吸收,请写出电解NaCl溶液的化学反应方程式___________。 _________________
_________________ ___________________________________
___________________________________ ______________。
______________。
 。
。 O2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2。环保工作人员在密闭系统中
O2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2。环保工作人员在密闭系统中 用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率。
用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率。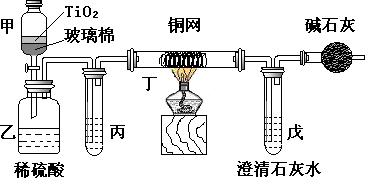
 液全部放入乙中,关闭活塞。回答下列问题:
液全部放入乙中,关闭活塞。回答下列问题: 成的气体除N2和CO2外,还有HCl及副产物Cl2等,上述实验是通过测定二氧化碳的量来确定对CN-的处理效果。则丙中加入的除杂试剂是__ __(填字母)
成的气体除N2和CO2外,还有HCl及副产物Cl2等,上述实验是通过测定二氧化碳的量来确定对CN-的处理效果。则丙中加入的除杂试剂是__ __(填字母)
 验中戊中共生成0.82 g沉淀,则该实验中测得CN-被处理的百分率等于___ _____,请说明该测得值与实际处理的百分率相比偏高还是偏低_ ___?简要说明可能的原因________________________ _________ _________。
验中戊中共生成0.82 g沉淀,则该实验中测得CN-被处理的百分率等于___ _____,请说明该测得值与实际处理的百分率相比偏高还是偏低_ ___?简要说明可能的原因________________________ _________ _________。