题目内容
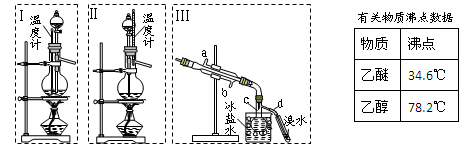
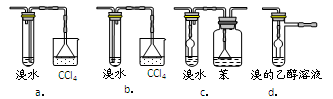
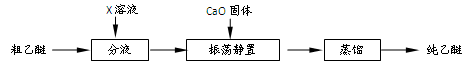
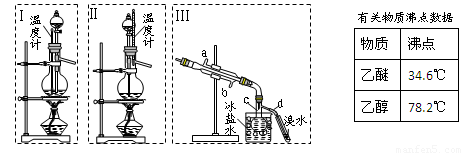
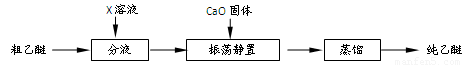
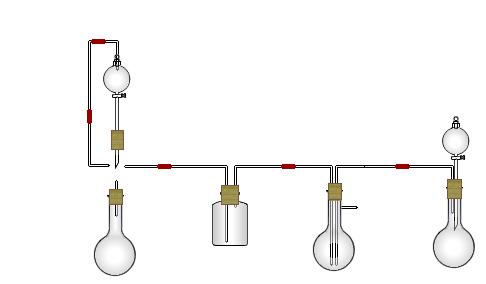
某实验小组用氨碱法制取碳酸钠的原理,在实验室设计下列模拟装置制备NaHCO3(铁架台、C装置水浴中的温度计、酒精灯等略去),然后再制取Na2CO3。提供的试剂有:硫酸、盐酸、石灰石、浓氨水、碳酸氢钾溶液、水、生石灰、食盐等。

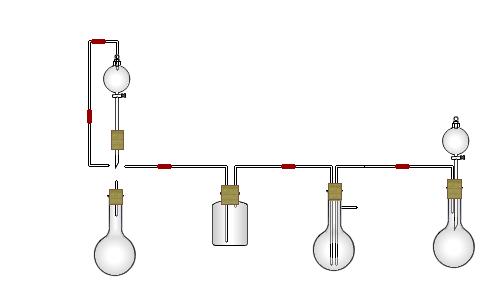
(1)在A中分液漏斗和烧瓶中加入的试剂分别是 、 ;D中分液漏斗和烧瓶中加入的试剂分别为 、 ;
(2) B中加入的试剂是 , 作用是 。
(3)写出C中生成的NaHCO3化学方程式: 。
(4)装置A中分液漏斗上方装一导管的主要作用是 。
(5)实验开始a、b两活塞的正确操作应是(选填序号) 。
①同时打开a、b两活塞 ②先打开a,后打开b ③先打开b,后打开a
(6)检验C装置溶液中生成的溶质是NaHCO3而不是Na2CO3的方法是 。
(7)由C中NaHCO3再制取Na2CO3需进行的实验操作有过滤、洗涤、 。
(8)从绿色化学角度看,这一装置的主要缺点是尾气逸出,浪费资源,
|
(本题12分;每空1分)
(1)盐酸 石灰石,浓氨水 生石灰
(2)碳酸氢钠溶液 除去氯化氢气体。
(3)NaCl + CO2 + NH3 + H2O → NaHCO3↓+ NH4Cl
(4)防止分液漏斗中挥发出的HCl逸出且使溶液容易滴下
(5)③ (6)取少量溶液加入氯化钡溶液若没有白色沉淀产生,说明是NaHCO3
(7)灼烧
(8)将尾气循环利用(或通入饱和食盐水中)

 阅读快车系列答案
阅读快车系列答案