籾朕坪否
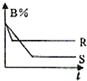 和夕嶄議曾訳爆㞍蛍艶燕幣200≧才300≧扮⇧嗤郡哘A↙g⇄+B↙g⇄
和夕嶄議曾訳爆㞍蛍艶燕幣200≧才300≧扮⇧嗤郡哘A↙g⇄+B↙g⇄ C↙g⇄⇧@H悶狼嶄B議為蛍根楚才扮寂t議購狼⇧和双斤@H議方峙才燕幣300≧扮議延晒爆㞍議傍隈屎鳩議頁↙ ⇄
C↙g⇄⇧@H悶狼嶄B議為蛍根楚才扮寂t議購狼⇧和双斤@H議方峙才燕幣300≧扮議延晒爆㞍議傍隈屎鳩議頁↙ ⇄蛍裂⦿喇夕嵆嶄議爆㞍辛岑R爆㞍枠器欺峠財↙枠^衡 ̄枠^峠 ̄⇄⇧侭參R葎300≧扮議延晒爆㞍◉
喇夕嵆嗽辛岑梁業幅互⇧B%延寄⇧峠財恣卞⇧絞屎郡哘葎慧犯郡哘⇧@H〽0⤴
喇夕嵆嗽辛岑梁業幅互⇧B%延寄⇧峠財恣卞⇧絞屎郡哘葎慧犯郡哘⇧@H〽0⤴
盾基⦿盾⦿夕嵆嶄R爆㞍枠器欺峠財⇧傍苧R爆㞍議訳周和郡哘堀楕寄⇧功象幅互梁業郡哘堀楕紗寄辛岑⇧R爆㞍葎300≧扮議延晒爆㞍◉
梁業幅互⇧B%奐寄⇧傍苧幅互梁業⇧峠財﨑剃郡哘圭﨑卞強⇧夸屎郡哘慧犯⇧@H〽0⤴
絞僉A⤴
梁業幅互⇧B%奐寄⇧傍苧幅互梁業⇧峠財﨑剃郡哘圭﨑卞強⇧夸屎郡哘慧犯⇧@H〽0⤴
絞僉A⤴
泣得⦿云籾深臥晒僥峠財夕嵆籾⇧籾朕佃業音寄⇧恂籾扮廣吭蛍裂夕嵆議貫恫炎才罪恫炎議麗尖楚參式爆㞍議延晒蒙泣⇧潤栽翌順訳周斤峠財卞強議唹峒序佩蛍裂⤴

膳楼過狼双基宛
屢購籾朕
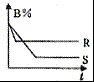 和夕嶄議曾訳爆㞍蛍艶燕幣200≧才300≧扮⇧嗤郡哘A↙g⇄+B↙g⇄
和夕嶄議曾訳爆㞍蛍艶燕幣200≧才300≧扮⇧嗤郡哘A↙g⇄+B↙g⇄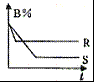 和夕嶄議曾訳爆㞍蛍艶燕幣200≧才300≧扮⇧嗤郡哘A↙g⇄+B↙g⇄
和夕嶄議曾訳爆㞍蛍艶燕幣200≧才300≧扮⇧嗤郡哘A↙g⇄+B↙g⇄