题目内容
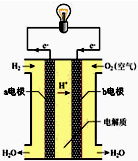 如果将该氧化还原反应设计成原电池装置,就可以把氢气中蕴含的化学能转化为电能,如图就是能够实现该转化的装置,被称为氢氧燃料电池.该电池的正极是
如果将该氧化还原反应设计成原电池装置,就可以把氢气中蕴含的化学能转化为电能,如图就是能够实现该转化的装置,被称为氢氧燃料电池.该电池的正极是分析:通入氢气的一极为原电池的负极,通入氧气的一极为原电池的正极,正极发生还原反应,负极发生氧化反应,结合电极方程式解答该题.
解答:解:氧气具有氧化性,通入氧气的一极为原电池的正极,正极发生还原反应,电极方程式为O2+4e-+4H+=2H2O,负极发生氧化反应,电极方程式为2H2-4e-=4H+,由电极方程式可知,当n(H2)=
=0.5mol时,转移电子1mol,个数为NA,
故答案为:b电极;O2+4e-+4H+=2H2O;NA.
| 11.2L |
| 22.4L/mol |
故答案为:b电极;O2+4e-+4H+=2H2O;NA.
点评:本题考查原电池和电解池知识,侧重于学生的分析能力的考查,为高频考点,注意把握电极方程式的书写,为解答该题的关键,同时注意电解质溶液为酸性的特点,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率.
能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率.
