题目内容
(14分)黄铁矿是我国大多数硫酸厂制取硫酸的主要原料。某化学兴趣小组对某黄铁矿石(主要成分为FeS)进行如下实验探究。
[实验一]:测定硫元素的含量
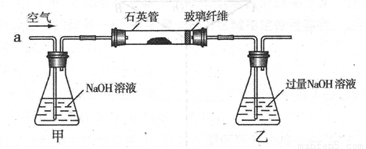
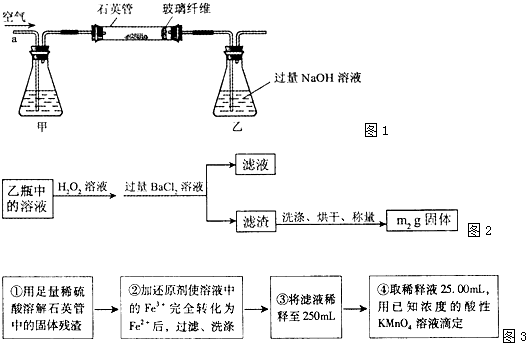
I.将mg该黄铁矿样品(杂质中不含硫和铁)放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通人空气,高温灼烧石英管中的黄铁矿样品至反应完全。石英管中发生反应的化学方程式为:

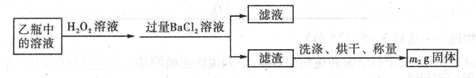
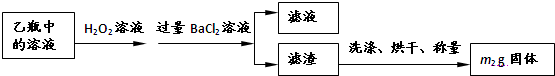
Ⅱ.反应结束后,将乙瓶中的溶液进行如下处理:

问题讨论:
(1)I中,甲瓶内所盛试剂是________溶液。乙瓶内发生反应的离子方程式有________________________、________________________________。
(2)Ⅱ中。所加HO溶液需足量的理由是________________。
(3)该黄铁矿石中硫元素的质量分数为________________。
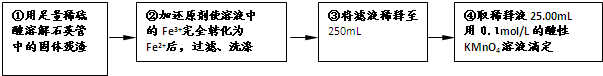
[实验二]:设计以下实验方案测定铁元素的含量

问题讨论:
(4)②中,若选用铁粉作还原剂。你认为合理吗? ________。若不合理,会如何影响测量结果:________(若合理,此空不答)。
(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有________。
(6)④中高锰酸钾溶液应放在_____滴定管中;判断滴定终点的现象为________________。
(14分)
(1)氢氧化钠(或氢氧化钾等)(2分)
 (2分)
(2分)  (2分)
(2分)
(2)使 完全氧化为
完全氧化为 (1分)
(1分)
 (或其他合理答案) (2分)
(或其他合理答案) (2分)
(4)不合理, 会使所测得的铁元素的质量分数偏大(2分)
(5)250mL容量瓶(1分)
(6)酸式、溶液恰好变为紫色,且半分钟不退去。(2分)
【解析】

 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案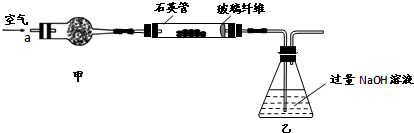


 2Fe2O3
+ 8SO2
2Fe2O3
+ 8SO2