题目内容
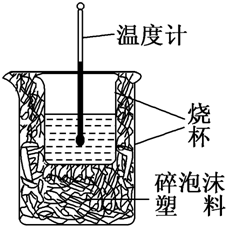 50ml0.50mol?L-1盐酸与50mL0.55mol?L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:
50ml0.50mol?L-1盐酸与50mL0.55mol?L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:(1)从实验装置上看,有两处缺点,其一是有处错误安装会导致热量散失较大,应该加
(2)烧杯间填满碎泡沫塑料的作用是
(3)若操作时分几次注入反应液,求得的反应热数值
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会
考点:中和热的测定
专题:实验题
分析:(1)大烧杯上如不盖硬纸板,会使一部分热量散失;根据量热计的构造来判断该装置的缺少仪器;
(2)中和热测定实验成败的关键是保温工作;
(3)操作时分几次注入反应液,导致热量散失;
(4)弱电解质电离吸收热量.
(2)中和热测定实验成败的关键是保温工作;
(3)操作时分几次注入反应液,导致热量散失;
(4)弱电解质电离吸收热量.
解答:
解:(1)大烧杯上如不盖硬纸板,会使一部分热量散失,求得的中和热数值将会减小;由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒,
故答案为:盖硬纸板;环形玻璃搅拌棒;
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是减少实验过程中的热量损失,
故答案为:减少实验过程中的热量损失;
(3)操作时分几次注入反应液,导致热量散失,求得的中和热数值将会减小;
故答案为:偏小;
(4)一水合氨为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量小于57.3kJ,故答案为:偏小.
故答案为:盖硬纸板;环形玻璃搅拌棒;
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是减少实验过程中的热量损失,
故答案为:减少实验过程中的热量损失;
(3)操作时分几次注入反应液,导致热量散失,求得的中和热数值将会减小;
故答案为:偏小;
(4)一水合氨为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量小于57.3kJ,故答案为:偏小.
点评:本题综合考查了中和热的测定、误差分析,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、用通入O2的方法来除去NO2中少量的NO |
| B、某无色溶液中加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有SO42- |
| C、向试管中滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口,试纸不变蓝,说明原溶液中无NH4+ |
| D、由于KNO3和KCl的溶解度随温度的变化差异较大,所以用重结晶的方法可除去KNO3固体中少量的KCl |
下列各组离子一定能大量共存的是( )
| A、在c(HCO3-)=0.1mol?L-1的溶液中:NH4+、Al3+、Cl-、NO3- |
| B、在与铝反应放出氢气的溶液中:K+、SO42-、Br-、Na+ |
| C、25℃,在由水电离出的c(H+)=10-13mol?L-1的溶液中:NH4+、Al3+、SO42-、NO3- |
| D、在能使甲基橙变红的溶液中:K+、Fe2+、Cl-、NO3- |
某种单烯烃经氢化后得到的饱和烃是CH3-CH(CH3)-CH2-CH(CH3)-CH3,该烯烃可能有的结构是( )种.
| A、1种 | B、2种 | C、3种 | D、4种 |
 根据中和热的测定实验填空.
根据中和热的测定实验填空.