题目内容
某元素的同位素
X,它的氯化物XCl2 1.11g溶于水制成溶液后,加入1mol/L的AgNO3溶液20mL恰好完全反应.若这种同位素原子核内有20个中子,求:
(1)Z值和A值;
(2)X元素在周期表中的位置;
(3)写出XCl2的电子式,并用电子式表示出XCl2的形成过程.
A Z |
(1)Z值和A值;
(2)X元素在周期表中的位置;
(3)写出XCl2的电子式,并用电子式表示出XCl2的形成过程.
分析:根据Cl-+Ag+═AgCl↓计算XCl2的物质的量,再由M=
计算其摩尔质量,摩尔质量与相对分子质量的数值相等,原子的质量数为原子的近似相对原子质量,结合该原子原子核内有20个中子,根据质子数=质量数-中子数来计算原子的质子数,利用质子数确定元素在周期表中的位置,并利用质量守恒定律及X的性质来书写反应方程式,推测现象.
| m |
| M |
解答:解:(1)由Cl-+Ag+═AgCl↓可知,n(Cl-)=n(Ag+)=0.02L×1mol/L=0.02mol,
n(XCl2)=
n(Cl-)=
×0.02mol=0.01mol,
则M(XCl2)=
=111g/mol,
所以XCl2相对分子质量为111,
所以X的相对原子质量=111-35.5×2=40,即X的质量数为40,
质子数=质量数-中子数=40-20=20,
答:Z=20,A=40;
(2)X为Ca,位于第四周期第ⅡA族,
答:X位于第四周期第ⅡA族;
(3)CaCl2的电子式: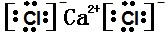 ;CaCl2的形成过程:
;CaCl2的形成过程: ,
,
答: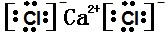 ,
, .
.
n(XCl2)=
| 1 |
| 2 |
| 1 |
| 2 |
则M(XCl2)=
| 1.11g |
| 0.01mol |
所以XCl2相对分子质量为111,
所以X的相对原子质量=111-35.5×2=40,即X的质量数为40,
质子数=质量数-中子数=40-20=20,
答:Z=20,A=40;
(2)X为Ca,位于第四周期第ⅡA族,
答:X位于第四周期第ⅡA族;
(3)CaCl2的电子式:
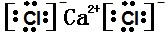 ;CaCl2的形成过程:
;CaCl2的形成过程: ,
,答:
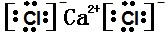 ,
, .
.点评:本题考查利用离子反应方程式的计算及确定元素在元素周期表中的位置、单质的性质等,题目难度不大,熟悉离子之间的关系、原子中的数量关系即可解答.

练习册系列答案
相关题目