题目内容
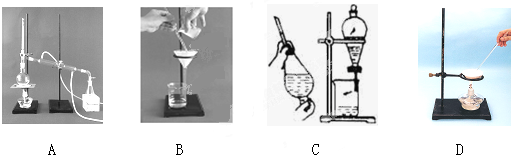
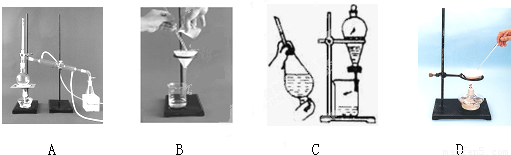
(1)下列A、B、C、D是中学常见的混合物分离或提纯的基本装置.
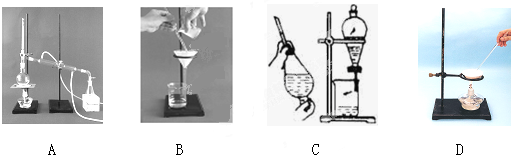
根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置(将A、B、C、D填入适当的空格中).
①除去Ca(OH)2溶液中悬浮的CaCO3
②从碘水中提取碘
③用自来水制取蒸馏水
④分离植物油和水
⑤除去食盐水中的泥沙
⑥与海水晒盐原理相符的是
(2)由可溶性铝盐制取氢氧化铝,需加入的试剂为:
白色的Fe(OH)2在空气中发生的颜色变化为

根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置(将A、B、C、D填入适当的空格中).
①除去Ca(OH)2溶液中悬浮的CaCO3
B
B
;②从碘水中提取碘
C
C
;③用自来水制取蒸馏水
A
A
;④分离植物油和水
C
C
;⑤除去食盐水中的泥沙
B
B
;⑥与海水晒盐原理相符的是
D
D
.(2)由可溶性铝盐制取氢氧化铝,需加入的试剂为:
氨水(或稀氨水)
氨水(或稀氨水)
;离子方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+
Al3++3NH3?H2O=Al(OH)3↓+3NH4+
.白色的Fe(OH)2在空气中发生的颜色变化为
白色迅速变为灰绿色最终变为红褐色
白色迅速变为灰绿色最终变为红褐色
.反应的化学方程式为:4Fe(OH)2+2H2O+O2═4Fe(OH)3
4Fe(OH)2+2H2O+O2═4Fe(OH)3
.分析:(1)A为蒸馏、B为过滤、C为萃取、分液、D为蒸发操作,结合混合物的性质的异同选择分离方法;
(2)氢氧化铝为两性物质,可与强碱反应,制备时应用弱碱;氢氧化亚铁不稳定,易与空气中氧气反应生成红褐色氢氧化铁.
(2)氢氧化铝为两性物质,可与强碱反应,制备时应用弱碱;氢氧化亚铁不稳定,易与空气中氧气反应生成红褐色氢氧化铁.
解答:解:(1)①除去Ca(OH)2溶液中悬浮的CaCO3应用过滤的方法分离;
②从碘水中提取碘可用萃取、分液的方法分离;
③用自来水制取蒸馏水可用蒸馏的方法;
④分离植物油和水可用分液的方法;
⑤除去食盐水中的泥沙可用过滤的方法;
⑥与海水晒盐原理相符的是蒸发,
故答案为:①B;②C;③A;④C;⑤B;⑥D;
(2)氢氧化铝为两性物质,可与强碱反应,制备时应用弱碱,可在铝盐中加入氨水,反应的离子方程式为
Al3++3NH3?H2O=Al(OH)3↓+3NH4+,白色的Fe(OH)2在空气中发生反应生成红褐色的氢氧化铁,现象是白色迅速变为灰绿色最终变为红褐色,反应的方程式为4Fe(OH)2+2H2O+O2═4Fe(OH)3,
故答案为:氨水(或稀氨水);Al3++3NH3?H2O=Al(OH)3↓+3NH4+;白色迅速变为灰绿色最终变为红褐色;4Fe(OH)2+2H2O+O2═4Fe(OH)3.
②从碘水中提取碘可用萃取、分液的方法分离;
③用自来水制取蒸馏水可用蒸馏的方法;
④分离植物油和水可用分液的方法;
⑤除去食盐水中的泥沙可用过滤的方法;
⑥与海水晒盐原理相符的是蒸发,
故答案为:①B;②C;③A;④C;⑤B;⑥D;
(2)氢氧化铝为两性物质,可与强碱反应,制备时应用弱碱,可在铝盐中加入氨水,反应的离子方程式为
Al3++3NH3?H2O=Al(OH)3↓+3NH4+,白色的Fe(OH)2在空气中发生反应生成红褐色的氢氧化铁,现象是白色迅速变为灰绿色最终变为红褐色,反应的方程式为4Fe(OH)2+2H2O+O2═4Fe(OH)3,
故答案为:氨水(或稀氨水);Al3++3NH3?H2O=Al(OH)3↓+3NH4+;白色迅速变为灰绿色最终变为红褐色;4Fe(OH)2+2H2O+O2═4Fe(OH)3.
点评:本题考查较为综合,涉及物质的分离操作以及相关物质的转化的性质的考查,题目难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
(1)下列A、B、C、D是中学常见的混合物分离或提纯的基本装置。
|
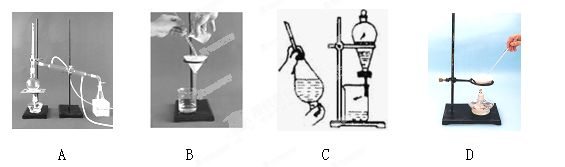 根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置(将A、B、C、D填入适当的空格中)。
根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置(将A、B、C、D填入适当的空格中)。①除去Ca(OH)2溶液中悬浮的CaCO3 ; ②从碘水中提取碘 ;
③用自来水制取蒸馏水 ; ④分离植物油和水 ;
⑤除去食盐水中的泥沙 ; ⑥与海水晒盐原理相符的是 。
(2)由可溶性铝盐制取氢氧化铝,需加入的试剂为: ;
离子方程式为: 。
白色的Fe(OH)2在空气中发生的颜色变化为 。
反应的化学方程式为: 。
(1)下列A、B、C、D是中学常见的混合物分离或提纯的基本装置。
|
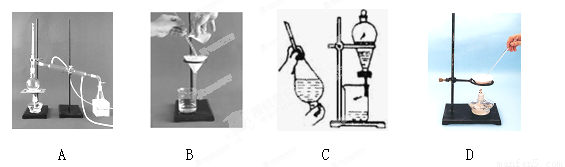
根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置(将A、B、C、D填入适当的空格中)。
①除去Ca(OH)2溶液中悬浮的CaCO3 ; ②从碘水中提取碘 ;
③用自来水制取蒸馏水 ; ④分离植物油和水 ;
⑤除去食盐水中的泥沙 ; ⑥与海水晒盐原理相符的是 。
(2)由可溶性铝盐制取氢氧化铝,需加入的试剂为: ;
离子方程式为: 。
白色的Fe(OH)2在空气中发生的颜色变化为 。
反应的化学方程式为: 。