题目内容
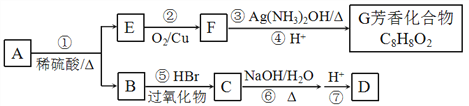
【题目】已知A的产量是衡量一个国家石油化工发展水平的标志,下图是由A为原料生产某些化工产品的转化关系图。

据此回答下列问题:
(1)写出A分子的结构简式:_________________
(2)写出B、C分子中,含氧基团的名称:B________ C___________
(3)写出下列反应类型:
①_________ ②____________ ③____________
(4)写出下列反应方程式:
②B→CH3CHO:___________________________
③B+C→D:______________________________
【答案】 CH2=CH2 羟基 羧基 加成反应 氧化反应 取代反应(或酯化反应) B→CH3CHO:2CH3CH2OH+O2![]() 2CH3CHO+ 2H2O CH3CH2OH+CH3COOH
2CH3CHO+ 2H2O CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
【解析】气体A的产量是衡量一个国家石油化工发展水平的标志,所以A是乙烯,结构简式为CH2=CH2,CH2=CH2和水发生加成反应生成乙醇,则B结构简式为CH3CH2OH,CH3CH2OH被氧化生成CH3CHO,CH3CHO被氧化生成C为CH3COOH,CH3CH2OH和CH3COOH发生酯化反应生成D为CH3COOCH2CH3。
(1)根据上面的分析可知,A的结构简式为CH2=CH2,故答案为:CH2=CH2;
(2) B为CH3CH2OH,含氧官能团为羟基;C为CH3COOH,含氧官能团为羧基,故答案为:羟基;羧基;
(3) 反应①是乙烯与水的加成反应;反应②为乙醇的催化氧化反应;反应③为乙醇和乙酸的酯化反应,故答案为:加成反应;氧化反应;取代反应(或酯化反应);
(4)反应②为乙醇的催化氧化,反应的方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O,是氧化反应,反应③为 CH3CH2OH和CH3COOH发生酯化反应生成CH3COOCH2CH3,反应的方程式为CH3COOH+CH3CH2OH
2CH3CHO+2H2O,是氧化反应,反应③为 CH3CH2OH和CH3COOH发生酯化反应生成CH3COOCH2CH3,反应的方程式为CH3COOH+CH3CH2OH![]() CH3COOC2H5+H2O,也是取代反应,
CH3COOC2H5+H2O,也是取代反应,
故答案为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O;氧化反应;CH3COOH+CH3CH2OH
2CH3CHO+2H2O;氧化反应;CH3COOH+CH3CH2OH![]() CH3COOC2H5+H2O。
CH3COOC2H5+H2O。

【题目】下列除去杂质的方法,正确的是
A. 苯中含有苯酚杂质:加入溴水,过滤
B. 溴乙烷中含有乙醇:加入浓氢溴酸,加热
C. 乙炔中含有硫化氢杂质:通入氯水中,洗气
D. 乙烯中含有乙醇杂质:通入水中,洗气
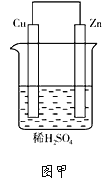
【题目】I.现用下图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量。量筒的规格为1000 mL,供选择的电极材料有纯铜片和纯锌片。请回答下列问题:

(1)b电极材料为__________,其电极反应式为_________________________。
(2)当量筒中收集到672 mL(标准状况下)气体时,通过导线的电子的物质的量为__________,此时a电极质量减少__________g。
II.某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的离子方程式有:________________________________;
(2)硫酸铜溶液可以加快氢气生成速率的原因是____________________________________;
(3)要加快上述实验中气体产生的速率,还可采取的措施有___________________(答两种);
(4)为了进一步研究硫酸铜的用量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。(假设混合溶液总体积等于混合前各溶液的体积之和)
实验 混合溶液 | A | B | C | D | E | F |
4 mol/L H2SO4 /mL | 30 | V1 | V2 | V3 | V4 | V5 |
饱和CuSO4溶液 /mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O /mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V3=____________, V8=______________;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因_____________________。
③实验A测得:收集到产生H2体积为112mL(标准状况下)时所需的时间为10分钟,求化学反应速率ν(H2SO4)=________________________(忽略反应前后溶液体积变化)。
p>