题目内容
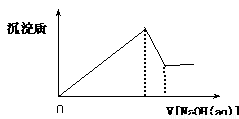
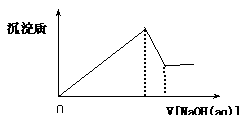
 向某溶液中逐滴加入0.5mol/L的NaOH溶液,生成沉淀的质量与加入NaOH溶液的体积之间的关系如右图所示,则该溶液中可能存在的离子是
向某溶液中逐滴加入0.5mol/L的NaOH溶液,生成沉淀的质量与加入NaOH溶液的体积之间的关系如右图所示,则该溶液中可能存在的离子是( )
| A、只有Al2+ | B、有Mg2+和Al3+ | C、有H+、Mg2+和Al3+ | D、有NH4+、Mg2+和Al3+ |
分析:Al3+和氢氧化钠反应生成氢氧化铝沉淀,氢氧化铝为两性氢氧化物,可溶于氢氧化钠中,Mg2+和氢氧化钠反应生成沉淀氢氧化镁,氢氧化镁不溶于碱,NH4+和碱反应放出氨气,不会生成沉淀,H+和氢氧化钠发生中和反应生成氯化钠和水.根据以上物质的性质结合图象分析.
解答:解:Al3+和氢氧化钠反应生成氢氧化铝沉淀,氢氧化铝为两性氢氧化物,可溶于氢氧化钠中,Mg2+和氢氧化钠反应生成沉淀氢氧化镁,氢氧化镁不溶于碱,NH4+和碱反应放出氨气,不会生成沉淀,H+和氢氧化钠发生中和反应生成氯化钠和水.从图象看出,随加入碱的量的增大,生成沉淀增多,故不会有氢离子,后发生沉淀部分溶解,说明一定含Mg2+和Al3+,中间加入氢氧化钠,沉淀不变,一定是和NH4+反应,故溶液中可能存在NH4+、Mg2+和Al3+,
故选D.
故选D.
点评:本题考查了离子的性质,要注意铝的氧化物和氢氧化物都为两性化合物,既可与酸反应又可与碱反应,分析图象要和物质的性质结合起来.

练习册系列答案
相关题目
向某溶液中逐滴加入0.5mol/L的NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积之间的关系如下图所示 ,则该溶液中可能存在的离子是 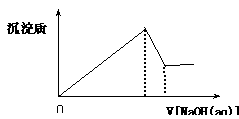
| A.只有Mg2+ | B.只有Al3+ |
| C.有H+、Mg2+和Al3+ | D.有Mg2+和Al3+ |
向某溶液中逐滴加入0.5mol/L的NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积之间的关系如下图所示 ,则该溶液中可能存在的离子是
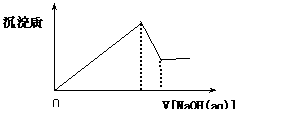 |
A.只有Mg2+ B.只有Al3+
C.有H+、Mg2+和Al3+ D.有Mg2+和Al3+