题目内容
已知:2Fe2++Br2====2Fe3++2Br-,若向100 mL的FeBr2溶液中通入标准状况下的Cl2 3.36 L,测得形成的溶液中c(Cl-)=c(Br-),则原FeBr2溶液的物质的量浓度为( )A.0.75 mol/L B.1.5 mol/L
C.2 mol/L D.3 mol/L
C
【解析】 本题考查氧化还原反应的顺序及依据方程式的计算。Cl2先与Fe2+反应,然后再与Br-反应。设FeBr2浓度为x moL/L。0.15×2=0.1 x+0.2 x-0.15×2,算得x=2。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
已知Br2+2Fe2+=2Fe3++2Br-,当向含1molFeBr2洛液中逐渐通入Cl2,溶液中有一半的Br-氧化时,下列判断不正确的是( )
| A、反应前后溶液的颜色发生了改变 | B、反应后溶液中c(Cl-)=C(Br-) | C、参加反应的Cl2为1 mol | D、反应的离子方程式为:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |

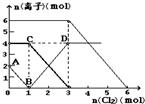 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2=2Fe3++2Br-;2Fe3++2I-=2Fe2++I2.则下列有关说法中,不正确的是( )
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2=2Fe3++2Br-;2Fe3++2I-=2Fe2++I2.则下列有关说法中,不正确的是( )
 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化情况如图所示.已知:2Fe2++Br2=2Fe3++2Br-,2Fe3++2I-=2Fe2++I2.则下列说法中不正确的是( )
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化情况如图所示.已知:2Fe2++Br2=2Fe3++2Br-,2Fe3++2I-=2Fe2++I2.则下列说法中不正确的是( )