题目内容
在常温下常压下,将16mL的H2、CH4、C2H2的混合气体与足量的氧气混合点燃,完全反应后,冷却到常温常压下,体积比原来缩小了26mL,则混合气体中CH4的体积为
| A.2mL | B.4mL | C.8mL | D.无法求解 |
B
根据化学反应方程式:CH4 + 2O2===== CO2 + 2H2O,可得每1 mL的CH4完全燃烧后,气体体积减少2mL;2H2 + O2===== 2H2O及2C2H2 + 5O2===== 4CO2 + 2H2O,这两个方程式中,每有1mL的H2、或C2H2完全燃烧,气体体积均减少3mL;
设:16mL的H2、CH4、C2H2的混合气体中,CH4有x mL,H2、和C2H2共有(16—x)mL;
即,2x+3/2(6-x)=26,得x=4
正确选项为B
设:16mL的H2、CH4、C2H2的混合气体中,CH4有x mL,H2、和C2H2共有(16—x)mL;
即,2x+3/2(6-x)=26,得x=4
正确选项为B

练习册系列答案
相关题目

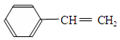 和 CH3-CH=CH2
和 CH3-CH=CH2 和
和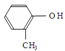
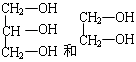

 状单烯烃,且与HBr加成的产物只有一种,试写出B与HBr反应的化学方程式 ▲ 。
状单烯烃,且与HBr加成的产物只有一种,试写出B与HBr反应的化学方程式 ▲ 。 写出C的结构简式 ▲ 。
写出C的结构简式 ▲ 。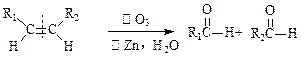 ;
;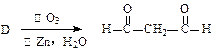 (唯一
(唯一 产物)
产物) 燃烧热为283KJ/mol。相同条件下,若2 molCH4燃烧生成液态水,所放出的热量为1mol CO完全燃烧放出热量的6.30倍,CH4完全燃烧反应的热化学方程式是
燃烧热为283KJ/mol。相同条件下,若2 molCH4燃烧生成液态水,所放出的热量为1mol CO完全燃烧放出热量的6.30倍,CH4完全燃烧反应的热化学方程式是  CO、CH4组成的混合气体在b ml O2中完全燃烧后,恢复到原温度和压强。
CO、CH4组成的混合气体在b ml O2中完全燃烧后,恢复到原温度和压强。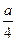 ml,则a与b关系的数学表达式是
ml,则a与b关系的数学表达式是 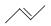 ,有一种有机物X它的键线式如下:
,有一种有机物X它的键线式如下: