��Ŀ����
ij��Һ���ܺ�������6�������е�ij���֣�Cl-��SO42-��HCO3-��Na+��K+��Mg2+���������ӵ�Ũ�Ⱦ���ȡ�Ϊ��ȷ����Һ����ɣ���������ʵ�飺
��ȡ100mL������Һ����������Ba(OH)2��Һ����Ӧ�������ˡ�ϴ�ӡ�����ó���4.88g��
��������м�����������ᣬ��2.33g�������ܽ⡣�����н��۲���ȷ����
A. ԭ��Һһ������SO42����HCO3����Mg2+�����ٴ���Na+��K+�е�һ��
B. ��Ҫ֤��ԭ��Һ���Ƿ���� Cl�������ڵڢٲ�����Һ�м������ữ���ټ���������Һ
C. ��Ba(OH)2��Һ��ʹԭ��Һ�е�����ǡ�÷�Ӧ����ȫ����ʱ�����Һ������
D. �ڢڲ�ʵ���й�����0.04mol HCl
��ϰ��ϵ�д�
 �ο�������ϵ�д�
�ο�������ϵ�д� ������ѧ��ʱ��ҵϵ�д�
������ѧ��ʱ��ҵϵ�д� ���������ʱ��ѵϵ�д�
���������ʱ��ѵϵ�д� �㽭�¿γ���άĿ�������ʱ��ѵϵ�д�
�㽭�¿γ���άĿ�������ʱ��ѵϵ�д�
�����Ŀ




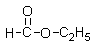

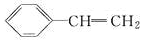
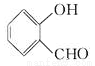
 2N2(g)+CO2(g)+2H2O(g) ��H=QkJ��mol-1��д��������Ӧ��ƽ�ⳣ������ʽ_______����֪�÷�Ӧ��ƽ�ⳣ��K���¶����߶���С����Q_______0���>����<����=������
2N2(g)+CO2(g)+2H2O(g) ��H=QkJ��mol-1��д��������Ӧ��ƽ�ⳣ������ʽ_______����֪�÷�Ӧ��ƽ�ⳣ��K���¶����߶���С����Q_______0���>����<����=������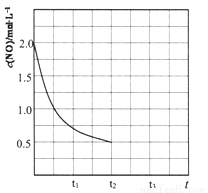
 2H++ClO-+Cl-
2H++ClO-+Cl-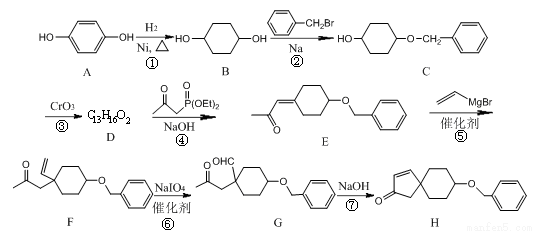
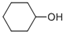 Ϊ�л�ԭ���Ʊ�
Ϊ�л�ԭ���Ʊ�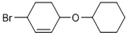 �ĺϳ�·������ͼ�����Լ����ã���ѡ���ʵ��л��ܼ����ϳ�·������ͼʾ����������ɣ�___________________��
�ĺϳ�·������ͼ�����Լ����ã���ѡ���ʵ��л��ܼ����ϳ�·������ͼʾ����������ɣ�___________________�� Fe2+��Cu2+
Fe2+��Cu2+ 2H+��Cl-��ClO-
2H+��Cl-��ClO-