题目内容
如下图所示,甲、乙之间的隔板K可以左右移动,甲中充入2 mol A和1 mol B,乙中充入2 mol C和1 mol He,此时K停在0处。在一定条件下发生可逆反应: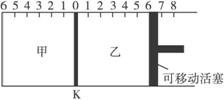
A.根据隔板K滑动与否可判断左右两边的反应是否达到平衡
B.达到平衡后,隔板K最终停留在左侧刻度0—2之间
C.到达平衡时,甲容器中的C的物质的量应大于乙容器中C的物质的量
D.若平衡时K停留在左侧1处,则活塞应停留在右侧6处
D 方程式两边气体的化学计量数之和不相等,所以A正确。该实验与先让甲乙达到平衡后再向乙中充入1 mol He等效,根据勒沙特列原理,K板向左移动,但不会到达刻度2,B正确。平衡时甲容器的体积小,C的物质的量多,C正确。若平衡时K停留在左侧1处,则活塞停留的刻度小于6,D错。

练习册系列答案
相关题目
有50mLNaOH溶液,向其中逐渐通入一定量的CO2,随后取此溶液100mL,并向此稀稀释后的溶液中逐滴加入0.1mol/L的HCl溶液,产生的
 |
CO2气体体积(标况)与所加入的盐酸的体积之间的关系如下图所示:
试分析NaOH在吸收CO2气体后,在甲、乙两种情况下,所得溶液中存在的溶质是什么?其物质的量之比是多少?产生的CO2气体体积(标况)是多少?