题目内容
【题目】25℃时,将浓度均为![]() 的
的![]() 溶液和
溶液和![]() 溶液按体积分别为Va和Vb混合,保持
溶液按体积分别为Va和Vb混合,保持![]() ,且生成的
,且生成的![]() 可溶于水。已知
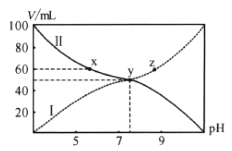
可溶于水。已知![]() 与混合液pH关系如图。下列说法错误的是( )
与混合液pH关系如图。下列说法错误的是( )
A.曲线Ⅰ表示![]() 溶液体积B.
溶液体积B.![]() 点存在
点存在![]()
C.电离平衡常数![]() D.向
D.向![]() 点溶液加入
点溶液加入![]() ,水的电离程度减小
,水的电离程度减小
【答案】C
【解析】
曲线I中体积为100mL时溶液的pH>7,呈碱性,曲线Ⅱ中溶液体积为100mL时溶液的pH<7,则曲线I表示的是BOH溶液,曲线Ⅱ表示的是HA溶液。
A. 根据分析可知,曲线Ⅰ表示![]() 溶液体积,曲线Ⅱ表示HA溶液体积,故A正确;
溶液体积,曲线Ⅱ表示HA溶液体积,故A正确;
B. 根据x点溶液中的电荷守恒可知:c(A-)+c(OH-)=c(B+)+c(H+),故B正确;
C. y点Va=Vb,二者恰好反应生成BA,此时溶液的pH>7,说明A-的水解程度大于B+,水解程度越大电离平衡常数越小,则电离平衡常数:K(HA)<K(BOH),故C错误;
D. 根据图象可知,z点BOH过量,向z点溶液加入NaOH,溶液中c(OH-)增大,导致水的电离程度减小,故D正确;
故选C。

练习册系列答案
相关题目