题目内容
(2011?佛山一模)一种甲醇、氧气和强碱溶液做电解质的新型手机电池,可连续使用一个月.该电池反应为:2CH3OH+3O2+4OH-
2CO32-+6H2O,则有关说法正确的是( )
| 放电 |
| 充电 |
分析:根据2CH3OH+3O2+4OH-
2CO32-+6H2O知,甲醇失去电子发生氧化反应,所以负极上是燃料发生失电子电极反应,CH3OH+8OH--6e-═CO32-+6H2O;氧气得电子发生还原反应,所以正极为氧气得电子发生还原反应,O2+2H2O+4e-═4OH-,根据电极反应式判断电极附近溶液的pH值变化.
| 放电 |
| 充电 |
解答:解:A、充电时是电解池的工作原理,阴极发生还原反应,故A错误;
B、放电时,负极上甲醇失电子发生氧化反应,甲醇失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为CH3OH+8OH--6e-═CO32-+6H2O,故B正确;
C、放电时,正极上的电极反应式为:O2+2H2O+4e-═4OH-,通入0.25mol氧气并完全反应后,有1mol电子转移,故C错误;
D、放电一段时间后,通入氧气的电极发生的电极反应为:O2+2H2O+4e-═4OH-,该电极附近溶液的pH升高,故D正确.
故选:BD.
B、放电时,负极上甲醇失电子发生氧化反应,甲醇失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为CH3OH+8OH--6e-═CO32-+6H2O,故B正确;
C、放电时,正极上的电极反应式为:O2+2H2O+4e-═4OH-,通入0.25mol氧气并完全反应后,有1mol电子转移,故C错误;
D、放电一段时间后,通入氧气的电极发生的电极反应为:O2+2H2O+4e-═4OH-,该电极附近溶液的pH升高,故D正确.
故选:BD.
点评:本题以燃料电池为载体考查了原电池原理,根据电池反应式判断正负极上发生反应的物质及电极附近溶液pH值的变化即可解答本题,难度较大.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
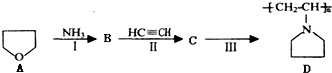

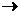


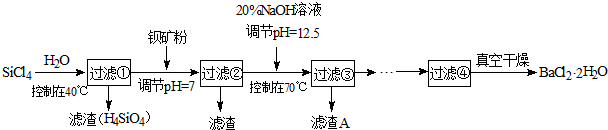
 (2011?佛山一模)纯碱、烧碱等是重要的化工原料.
(2011?佛山一模)纯碱、烧碱等是重要的化工原料.