题目内容
150℃时,1L混合烃与9L氧气混合,在密闭容器内充分燃烧,当恢复到150℃时,容器内压强增大8%,则该混合烃的组成是
| A.甲烷:乙烷=1:1 | B.丙炔:乙炔=1:4 |
| C.乙烯:丁烷=1:4 | D.乙烯:丁烯=1:4 |
D
烃在氧气中充分燃烧的方程式为: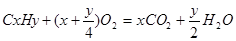 ,由该方程式分析可知,温度在150℃时,当y=4时,该反应为等体积反应;当y<4时,反应为气体体积减小的反应;当y>4时,反应为气体体积增大的反应。在A、B、C、D四个选项中,甲烷、丙炔、乙烯分子中H原子均4个,所以,解此题的关键是分析乙烷、乙炔、丁烷、丁烯的反应情况,首先排除B选项,乙炔分子中H只有2个属于反应后气体体积减小的反应。
,由该方程式分析可知,温度在150℃时,当y=4时,该反应为等体积反应;当y<4时,反应为气体体积减小的反应;当y>4时,反应为气体体积增大的反应。在A、B、C、D四个选项中,甲烷、丙炔、乙烯分子中H原子均4个,所以,解此题的关键是分析乙烷、乙炔、丁烷、丁烯的反应情况,首先排除B选项,乙炔分子中H只有2个属于反应后气体体积减小的反应。
反应后容器内压强增大8%即物质的量增大(1+9)8%=0.8mol
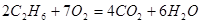 物质的量增大△n
物质的量增大△n
2 7 4 6 1
0.5 0.25
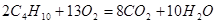 物质的量增大△n
物质的量增大△n
2 13 8 10 3
0.8 1.2
 物质的量增大△n
物质的量增大△n
1 6 4 4 1
0.8 0.8
所以正确选项为D
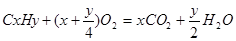 ,由该方程式分析可知,温度在150℃时,当y=4时,该反应为等体积反应;当y<4时,反应为气体体积减小的反应;当y>4时,反应为气体体积增大的反应。在A、B、C、D四个选项中,甲烷、丙炔、乙烯分子中H原子均4个,所以,解此题的关键是分析乙烷、乙炔、丁烷、丁烯的反应情况,首先排除B选项,乙炔分子中H只有2个属于反应后气体体积减小的反应。
,由该方程式分析可知,温度在150℃时,当y=4时,该反应为等体积反应;当y<4时,反应为气体体积减小的反应;当y>4时,反应为气体体积增大的反应。在A、B、C、D四个选项中,甲烷、丙炔、乙烯分子中H原子均4个,所以,解此题的关键是分析乙烷、乙炔、丁烷、丁烯的反应情况,首先排除B选项,乙炔分子中H只有2个属于反应后气体体积减小的反应。反应后容器内压强增大8%即物质的量增大(1+9)8%=0.8mol
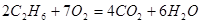 物质的量增大△n
物质的量增大△n2 7 4 6 1
0.5 0.25
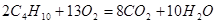 物质的量增大△n
物质的量增大△n2 13 8 10 3
0.8 1.2
 物质的量增大△n
物质的量增大△n1 6 4 4 1
0.8 0.8
所以正确选项为D

练习册系列答案
 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
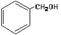 酚类 –OH
酚类 –OH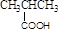 羧酸 –CHO
羧酸 –CHO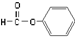 醛类 –CHO
醛类 –CHO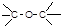
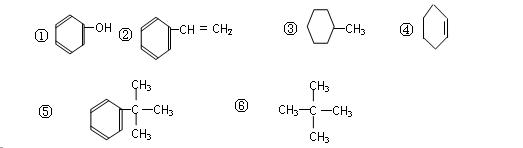

 取一定量的这些烃完全燃烧后,生成m摩CO2和n摩水,依下述条件,填入相应烃的序号:
取一定量的这些烃完全燃烧后,生成m摩CO2和n摩水,依下述条件,填入相应烃的序号: