题目内容
(1)研究证明使用氯气作自来水消毒剂时,氯气会与水中有机物反应,生成CHCl3等物质,这些物质可能是潜在的致癌致畸物质。目前人们已研发出多种自来水的新型消毒剂。下列物质不能作自来水消毒剂的是
_________ (填序号)。
A.硫酸铜 B.二氧化氯 C.臭氧 D.硫酸亚铁
(2)高铁(VI)酸盐(如Na2FeO4)是新一代水处理剂。其制备方法有:次氯酸盐氧化法(湿法)和高温过氧化物法(干法)等。湿法是在碱性溶液中用次氯酸氧化铁盐(Ⅲ),写出该法的离子方程式:______________________。
(3)用高铁(VI)酸盐设计的高铁(VI)电池是一种新型可充电电池,电解质为KOH溶液,放电时的总反应:
3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH。
①写出正极发生的电极反应式:_________________。
②用高铁(VI)电池作电源,以石墨作阳极,以Cu作阴极,对足量KOH溶液进行电解,当电池中有0.2 mol K2FeO4反应时,则在电解池中生成______L H2(标准状况)。
③下表列出了某厂排放的废水中锌的含量及国家环保标准值的有关数据
_________ (填序号)。
A.硫酸铜 B.二氧化氯 C.臭氧 D.硫酸亚铁
(2)高铁(VI)酸盐(如Na2FeO4)是新一代水处理剂。其制备方法有:次氯酸盐氧化法(湿法)和高温过氧化物法(干法)等。湿法是在碱性溶液中用次氯酸氧化铁盐(Ⅲ),写出该法的离子方程式:______________________。
(3)用高铁(VI)酸盐设计的高铁(VI)电池是一种新型可充电电池,电解质为KOH溶液,放电时的总反应:
3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH。
①写出正极发生的电极反应式:_________________。
②用高铁(VI)电池作电源,以石墨作阳极,以Cu作阴极,对足量KOH溶液进行电解,当电池中有0.2 mol K2FeO4反应时,则在电解池中生成______L H2(标准状况)。
③下表列出了某厂排放的废水中锌的含量及国家环保标准值的有关数据
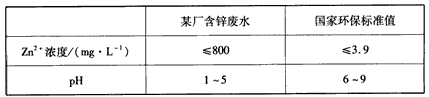
该厂只用调节pH的方法处理废水,当调整pH=7时,此时废水中Zn2+的浓度为__________mg/L,_______ (填“符合”或“不符合”)国家环保标准(常温下,Ksp[Zn(OH)2]=1.2×10-17)。
(1)AD
(2)10OH-+3ClO-+2Fe3+=3Cl-+2FeO42-+5H2O
(3)①FeO42-+4H2O+3e-=Fe(OH)3↓+5OH-;②6.72;③78;不符合
(2)10OH-+3ClO-+2Fe3+=3Cl-+2FeO42-+5H2O
(3)①FeO42-+4H2O+3e-=Fe(OH)3↓+5OH-;②6.72;③78;不符合

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
| |||||||||||||||||||

