题目内容
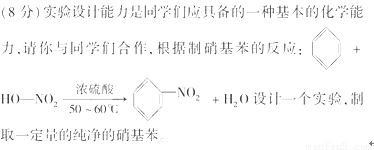
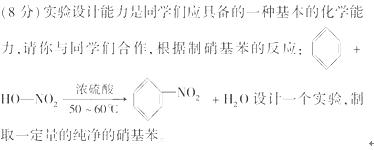
相关物质性质如下表所示:
|
物质 |
熔点/℃ |
沸点/℃ |
相对密度(20℃) |
毒性 |
水溶性 |
|
苯 |
5.5 |
80.1 |
0.8794 |
有 |
不溶于水 |
|
硝酸 |
-41.59 |
83 |
1.503 |
|
易溶于水 |
|
硝基苯 |
5.7 |
210.9 |
1.205 |
有 |
不溶于水 |
可供选择的实验用品:
①仪器:烧杯、大试管、铁架台(带铁圈)、石棉网、酒精灯、橡皮塞、玻璃管、温度计、分液漏斗等。
②药品:浓硝酸、稀硝酸、浓硫酸、稀硫酸、苯、5%NaOH溶液、蒸馏水等。
请参考以下实验设计思路,讨论并回答有关问题。
(2)选择合适的实验仪器及条件
①采用的加热方式:
________________________________________________________________________,
其优点是
________________________________________________________________________。
②反应物均为________,采用________作反应器。
③反应过程中由于有易挥发的物质,为防止损失采用________,其兼起________作用。
④用________来控制________的温度。
⑤请画出实验装置简图。
(2)安排合理的实验步骤
①按装置图组装好实验仪器。
②在大试管里,先加入1.5 mL浓硝酸和2 mL浓硫酸,摇匀,冷却到50~60℃。
③再慢慢滴入1 mL苯,不断轻轻摇动,使之混合均匀,塞好单孔塞。
④放在50~60℃的水浴中加热10 min。
(3)产品提纯
探究讨论:①浓硝酸和浓硫酸的混合顺序能否颠倒?为什么?
________________________________________________________________________。
②浓硫酸的作用是
________________________________________________________________________。
(1)①水浴加热'便于控制温度,受热均匀'②液体'大试管'③长玻璃管'冷凝回流'④温度计'水浴
⑤
(3)①不能。浓硝酸的密度比浓硫酸的小,若向浓硫酸中加浓硝酸,浓硝酸会浮在浓硫酸的表面上,浓硫酸溶于水放出大量热,造成溶液局部沸腾,外溅造成事故
②催化剂、吸水剂
【解析】设计化学实验的依据是化学原理。根据客观条件设计切实可行且装置简单、操作方便的最佳方案。
从本题的反应原理知反应物均为液体且苯易挥发,浓硝酸受热不稳定,苯及硝基苯均有毒,浓硫酸溶于水要放出大量的热,因此对实验要求较高,特别是对温度的控制是影响整个实验成败的关键,采用水浴加热是最佳的选择,冷凝回流装置也是提高实验效果的有效措施。

 发散思维新课堂系列答案
发散思维新课堂系列答案
相关物质性质如下表所示:
| 物质 | 熔点/℃ | 沸点/℃ | 相对密度(20℃) | 毒性 | 水溶性 |
| 苯 | 5.5 | 80.1 | 0.8794 | 有 | 不溶于水 |
| 硝酸 | -41.59 | 83 | 1.503 |
| 易溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 有 | 不溶于水 |
可供选择的实验用品:
①仪器:烧杯、大试管、铁架台(带铁圈)、石棉网、酒精灯、橡皮塞、玻璃管、温度计、分液漏斗等。
②药品:浓硝酸、稀硝酸、浓硫酸、稀硫酸、苯、5%NaOH溶液、蒸馏水等。
请参考以下实验设计思路,讨论并回答有关问题。
(2)选择合适的实验仪器及条件
①采用的加热方式:
________________________________________________________________________,
其优点是
________________________________________________________________________。
②反应物均为________,采用________作反应器。
③反应过程中由于有易挥发的物质,为防止损失采用________,其兼起________作用。
④用________来控制________的温度。
⑤请画出实验装置简图。
(2)安排合理的实验步骤
①按装置图组装好实验仪器。
②在大试管里,先加入1.5 mL浓硝酸和2mL浓硫酸,摇匀,冷却到50~60℃。
③再慢慢滴入1 mL苯,不断轻轻摇动,使之混合均匀,塞好单孔塞。
④放在50~60℃的水浴中加热10 min。
(3)产品提纯
探究讨论:①浓硝酸和浓硫酸的混合顺序能否颠倒?为什么?
________________________________________________________________________。
②浓硫酸的作用是
________________________________________________________________________。
某小组同学欲研究SO2的性质。
(1)将相关的含硫物质分为如下表所示3组,第2组中物质X的化学式是 。
| 第1组 | 第2组 | 第3组 |
| S(单质) | SO2、X、Na2SO3、NaHSO3 | SO3、H2SO4、Na2SO4、NaHSO4 |
(熔点:SO2 -76.1℃,SO3 16.8℃;沸点:SO2 -10℃,SO3 45℃)

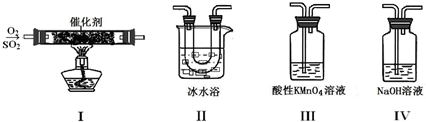
①装置Ⅰ模拟工业生产中SO2催化氧化的反应,其化学方程式是 。
②甲同学按Ⅰ、Ⅱ、Ⅲ、Ⅳ的顺序连接装置,装置Ⅱ的作用是 ;装置Ⅲ中溶液逐渐褪色,生成Mn2+,同时pH降低,则该反应的离子方程式是 。
③乙同学按Ⅰ、Ⅱ、Ⅳ的顺序连接装置,若装置Ⅳ中有40 mL 2.5mol/L NaOH溶液,反应后增重4.8 g,则装置Ⅳ中发生反应的化学方程式是 。