��Ŀ����
����Ŀ�������ױ��� ����һ����ȼ��������ˮ����ˮ�ܶ�С���ж�Һ�壬����Ҫ���л�����ԭ�ϣ���Ҫ�����Ʊ��ϳ���֬�����������ȡ�
����һ����ȼ��������ˮ����ˮ�ܶ�С���ж�Һ�壬����Ҫ���л�����ԭ�ϣ���Ҫ�����Ʊ��ϳ���֬�����������ȡ�
��1�������ױ����ڱ���ͬϵ�ѡ��һ���Լ����𱽺;����ױ�����Һ�壬�����Լ���_____________________��
��2�������ױ������е�һ����ԭ�ӱ���ԭ��ȡ�����ò�����__________�֡�
��3�������谷�� ��Ҳ��һ����Ҫ�Ļ���ԭ�ϣ���ṹ�ɿ��������ױ������еIJ���̼ԭ�ӱ�Nԭ���û����á������谷�ķ���ʽ_____________����˴Ź���������________���壬��������������Ϊ_____________��
��Ҳ��һ����Ҫ�Ļ���ԭ�ϣ���ṹ�ɿ��������ױ������еIJ���̼ԭ�ӱ�Nԭ���û����á������谷�ķ���ʽ_____________����˴Ź���������________���壬��������������Ϊ_____________��
���𰸡� ���Ը��������Һ 2 C3H6N6 1 66.7%
�������������������1��������ʹ���Ը��������Һ��ɫ������ͬϵ����ʹ���Ը��������Һ��ɫ��
��2�������ױ��������ĶԳƣ���2�ֵ�Ч����
��3�����������谷�ṹ��ʽ��д�����谷�ķ���ʽ��ֻ��1�ֵ�Ч����
������ ��1��������ʹ���Ը��������Һ��ɫ������ͬϵ����ʹ���Ը��������Һ��ɫ�������ø��������Һ���𱽺;����ױ�����Һ�塣
��2�������ױ������е�һ����ԭ�ӱ���ԭ��ȡ�����ò�����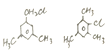 ����2�֡�
����2�֡�
��3�������谷�ķ���ʽC3H6N6��ֻ��1�ֵ�Ч������˴Ź���������1���壬��������������Ϊ![]() 66.7%��
66.7%��

����Ŀ�������������NOx������Ⱦ�ǻ�ѧ�о�����Ҫ����֮һ��NO�ܱ����յ����ۻ�ԭΪN2��ͬʱ����ͬʱ����FeO����������װ��ģ��÷�Ӧ��

��֪����Ũ���������NO����NaOH��Һ����NO2��Ӧ������NO��Ӧ��
��1������װ�ýӿڵ�����˳��Ϊa��__________��������������Сд��ĸ��ʾ����
��2��װ��D��������___________________��
��3��װ��E�з�Ӧ�Ļ�ѧ����ʽΪ___________________��
��4����Һ©����������ƿ�й۲쵽��ʵ��������_____________________��
��5��ʵ���ҳ���NaOH��Һ���ն���ĵ�������(NOx)��NO+NO2+2NaOH=2NaNO2+H2O�����ʵ����֤����NaNO2�������������л�ԭ�ԡ�
��ѡ�Լ���ϡ���ᡢKI-������Һ��˫��ˮ�����Ը��������Һ
ʵ�鲽�� | ʵ����� | ���� | ʵ����� |
1 | __________ | __________ | NaNO2���������� |
2 | __________ | __________ | NaNO2���л�ԭ�� |
��6�����յõ����������ƣ�NaNO2)�����ʳ�ηdz����ƣ����Խ�ǿ��
��֪��Ksp(AgNO2) =2.0��10-8��Ksp(AgCl) =1.8��10-10��
�� Ka(HNO2) =5.1��10-4��
������NaNO2��NaCl���ֹ��壬ʵ�鷽����__________________________���Լ���ѡ����
����Ŀ��ijͬѧ��Cl2��KI��Һ�ķ�Ӧ������ʵ��̽������Ӧװ�����£�

ͨ������һ��ʱ�䣬KI��Һ��Ϊ��ɫ������ͨ������һ��ʱ�����Һ��ɫ��ȥ����Ϊ��ɫ������ͨ�������������Һ��Ϊdz����ɫ��
��1����֪I2��I��![]() I3�� �� I2��I3����ˮ�����ʻ�ɫ��Ϊȷ����ɫ��Һ�ijɷ֣�����������ʵ�顣
I3�� �� I2��I3����ˮ�����ʻ�ɫ��Ϊȷ����ɫ��Һ�ijɷ֣�����������ʵ�顣
���� | ʵ������ | |
a | ȡ2~3 mL��ɫ��Һ����������CCl4�� ���á� | CCl4����Ϻ�ɫ�� ˮ����dz��ɫ�� |
b | ȡ2~3 mL���͵�ˮ����������CCl4�� ���á� | CCl4����Ϻ�ɫ��ˮ�㼸����ɫ�� |
�� ʵ��b��Ŀ���� ��
�� ����ʵ��a�У�ˮ���к��е������� ��
�� ʵ��a��ˮ��Һ��ɫ��dz��ԭ���� ��
�� Ϊ��֤ʵ����Ͻ��ԣ���ʵ��a��b�Ļ����ϣ��貹��һ��ʵ�飬��ʵ��Ϊ ��
��2��ͨ����������Һ�ɻ�ɫ��Ϊ��ɫ������Ϊ������I2��������֪1 mol Cl2������0��2 mol I2���÷�Ӧ�Ļ�ѧ����ʽ�� ��
��3�� ��������ʵ�飬��Ԥ�������-KI��Һ�г���ͨ�����������ܹ۲쵽������Ϊ ��
