题目内容
【题目】下列有关热化学反应的描述正确的是( )
A.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol
B.CO的燃烧热ΔH=-283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g) ΔH=(2×283.0)kJ/mol
C.已知:C(s)+O2(g)=CO2(g)△H1;C(s)+![]() O2(g)=CO(g)△H2 ,则△H1>△H2
O2(g)=CO(g)△H2 ,则△H1>△H2
D.C(石墨,s)= C(金刚石,s) ΔH=+1.9kJ·mol-1 ,则金刚石比石墨稳定
【答案】B
【解析】
A.中和热是强酸强碱稀溶液完全中和生成1mol水时所释放的能量,H2SO4和Ca(OH)2反应不仅生成水,还生成硫酸钙的沉淀,放出能量更多,ΔH<2×(-57.3)kJ/mol,A错误;
B.燃烧热是1mol纯物质完全燃烧生成稳定的氧化物所释放的能量,CO(g)+1/2O2(g)=CO2(g) ΔH=-283.0kJ/mol,当反应逆向进行时,其反应热与正反应的反应热数值相等,符号相反,则2CO2(g)=2CO(g)+O2(g) ΔH=(2×283.0)kJ/mol,B正确;
C.C(s)+O2(g)=CO2(g)△H1<0 ;C(s)+![]() O2(g)=CO(g)△H2<0 ,
O2(g)=CO(g)△H2<0 ,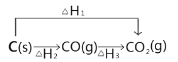 ,△H2+△H3=△H1,△H1<0,△H2<0 , △H3<0 ,所以△H1<△H2,C错误;
,△H2+△H3=△H1,△H1<0,△H2<0 , △H3<0 ,所以△H1<△H2,C错误;
D.由C(石墨,s)= C(金刚石,s) ΔH=+1.9kJ·mol-1 ,可知1mol石墨的总能量比1mol金刚石总能量低,则石墨比金刚石稳定,D错误;故答案为:B。

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目